Що спричиняє інсулінорезистентність, що лежить в основі ожиріння?
Ольга Т. Харді
програма з молекулярної медицини, Медична школа Університету Массачусетсу, Вустер, штат Массачусетс, США
b Департамент педіатрії, Медичний факультет Університету Массачусетсу, Вустер, штат Массачусетс, США
Михайло П. Чех
програма з молекулярної медицини, Медична школа Університету Массачусетсу, Вустер, штат Массачусетс, США
Сільвія Корвера
програма з молекулярної медицини, Медична школа Університету Массачусетсу, Вустер, штат Массачусетс, США
Анотація
Мета огляду
Асоціація між ожирінням та резистентністю до інсуліну представляє велику зацікавленість та величезний вплив на громадське здоров'я, оскільки протягом останнього року сотні статей були опубліковані, присвячені можливим механізмам, що лежать в основі цієї асоціації. Метою цього огляду є висвітлення деяких ключових останніх літературних джерел з акцентом на нові концепції.
Останні висновки
Продовжує виявлятись специфічний зв’язок між накопиченням вісцеральної жирової тканини та резистентністю до інсуліну. Ожиріння внутрішніх органів корелює із накопиченням надлишків ліпідів у печінці та призводить до автономного порушення клітин у передачі сигналів інсуліну. Вісцеральна жирова тканина також схильна до запалення та вироблення запальних цитокінів, що також сприяє погіршенню сигналізації інсуліну. Розширення вісцеральної жирової тканини та надмірне накопичення ліпідів у печінці та м’язах може бути наслідком обмеженої можливості розширення підшкірної жирової тканини через властивості її позаклітинного матриксу та здатності до капілярного росту.
Резюме
Недавні дослідження підкреслюють необхідність більш глибокого розуміння механізмів, що пов'язують ожиріння вісцеральної системи з накопиченням жиру в печінці, механізми, за допомогою яких накопичення ектопічного жиру викликає резистентність до інсуліну, та механізми, за допомогою яких визначається розмір депо жирової тканини.
ВСТУП
Інсулінорезистентність є необхідним попередником для розвитку цукрового діабету 2 типу (T2DM) і пов'язана з гіпертонією та дисліпідемією [1]. Епідеміологічні дані пов'язують T2DM із ожирінням, а причинно-наслідковий зв'язок між резистентністю до інсуліну та збільшенням ваги визначається в класичних дослідженнях, в яких худі особи, що не мали ожиріння або діабету в анамнезі, стали експериментально стійкими до інсуліну [2]. Ці факти підтверджують велике значення розуміння фізіологічних основ стійкості до інсуліну при ожирінні.
НЕ ВСІ ФОРМИ ОЖИРЕННЯ РЕЗУЛЬТУЮТЬ ІНСУЛІНОВУ СТІЙКІСТЬ
У цьому контексті механізми, що контролюють можливість розширення підшкірної жирової тканини, включаючи її високу здатність до диференціації адипоцитів та зберігання ліпідів, можуть бути ключовими факторами для визначення ризику діабету при ожирінні [7]. Підвищена здатність до утворення адипоцитів, передбачається наявністю гіперплазії в підшкірній жировій клітковині [8], корелює зі зниженням ризику порушень рівня глюкози та інсуліну. Крім того, закономірності експресії генів підшкірної жирової тканини відрізняються більше, ніж моделі експресії генів скелетних м’язів при порівнянні інсуліночутливих та інсулінорезистентних осіб. Ці результати узгоджуються з варіаціями підшкірної жирової тканини, яка є ключовим фактором у визначенні ризику метаболічних захворювань. Встановлено, що ці відмінності включають гени, пов’язані з метаболізмом ліпідів та жирних кислот, запаленням та регуляцією клітинного циклу [9▪].
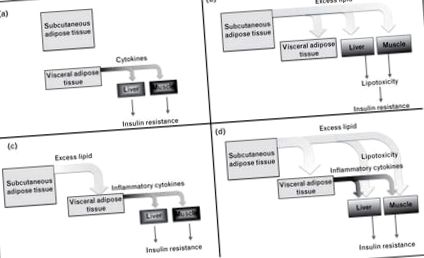
Чому накопичення вісцерального жиру пов’язане з резистентністю до інсуліну? Однією з можливостей є те, що вісцеральний жир сам по собі є діабетогенним, наприклад, він виділяє адипокіни, які погіршують чутливість до інсуліну в таких тканинах, як печінка та м’язи, які збільшуються при розширенні цього депо (рис. 1а). Інша можливість полягає в тому, що накопичення вісцерального жиру є сурогатним показником ектопічного накопичення ліпідів та ліпотоксичності, які паралельно відбуваються в печінці та м’язах, викликаючи резистентність до інсуліну в цих тканинах (рис. 1b). Третя можливість полягає в тому, що надлишкове накопичення ліпідів у вісцеральній жировій тканині насправді спричинює набуття діабетогенних властивостей (рис. 1в); вісцеральна жирова тканина дійсно накопичує макрофаги, які вивільняють запальні цитокіни, що може погіршити чутливість до інсуліну. Четверта можливість - така, при якій ліпотоксичність у периферичних тканинах та вироблення цитокінів у вісцеральній жировій тканині сприяють системній резистентності до інсуліну (рис. 1г). Останні дані, пов’язані з цими моделями, розглядаються нижче.
Потенційні механізми, за допомогою яких ожиріння внутрішніх органів може бути пов’язане з резистентністю до інсуліну. Опис кожної моделі міститься в тексті.
ВИЗНАЧЕННЯ ІНСУЛІНОВОЇ ОПОРНОСТІ
Системну інсулінорезистентність можна виміряти як знижену швидкість утилізації глюкози у гризунів та людей у відповідь на визначені концентрації інсуліну [1]. Системна інсулінорезистентність може бути наслідком порушення дії інсуліну в метаболічно активних органах і тканинах, включаючи скелетні м’язи, печінку та жирову тканину. Ступінь, до якої системна інсулінорезистентність обумовлена порушенням дії інсуліну в скелетних м'язах, печінці або жировій тканині, може відрізнятися у різних осіб.
У скелетних м’язах резистентність до інсуліну проявляється як зменшення транспорту глюкози та зниження синтезу м’язового глікогену у відповідь на циркулюючий інсулін. Чутливість до інсуліну знижується в міоцитах, отриманих від людей із ожирінням, або культивованих міоцитах у присутності ліпідів, похідних адипоцитів [10], що підтримує концепцію, що накопичення надлишків ліпідів або їх метаболічних похідних спричинює зниження сигналізації інсуліну в скелетних м'язах [11,12] . Нещодавно м’язова резистентність до інсуліну у людей із ожирінням, що страждають на цукровий діабет, також корелювала зі зменшенням транскапілярного транспорту інсуліну [13 cross.tv] і виявила, що він присутній у мишей, що містять специфічні для ендотеліальних клітин дефекти сигналізації інсуліну [14 cross.tv]. Залишається визначити, чи спричиняє ожиріння стійкість ендотеліальних клітин до інсуліну в м’язах. Інсулінорезистентність також корелює з дефіцитом мітохондріального дихального ланцюга в м'язах [15], але це може бути наслідком, а не причиною інсулінорезистентності [16▪].
У печінці інсулінорезистентність є вибірковою, оскільки інсулін не пригнічує глюконеогенез, але продовжує стимулювати синтез жирних кислот [17]. Таким чином, точка, в якій сигналізація про інсулін порушується при ожирінні, знаходиться за активацією рецептора інсуліну. Критична роль ссавців-мішеней комплексу рапаміцину (mTORC) у печінковому ліпогенезі [18], а також інших механізмів після серин-треонін-протеїнкінази Akt2 [19▪] може бути відповідальною за це роз'єднання метаболізму глюкози та ліпідів у сигнальний шлях інсуліну, який в кінцевому рахунку проявляється як гіперглікемія та гіпер-тригліцеридемія.
У жировій тканині інсулінорезистентність проявляється як порушення стимульованого інсуліном транспорту глюкози, а також як порушення інгібування ліполізу. Як і в печінці, адипоцити демонструють розбіжності в передачі сигналів інсуліну, завдяки чому ефект інсуліну на торгівлю глюкозою-4 притупляється, проте його вплив на ядерне виключення Forkhead Box O-1 (FoxO1) зберігається [20]. Ожиріння може спричинити резистентність до інсуліну до адипоцитів за допомогою клітинних автономних механізмів або, як детально описано нижче, через взаємодію між адипоцитом та медіаторами запалення.
ВИРОБНИЦТВО ВИРОБНИХ ЦІТОКІНІВ ТКАНИН ТАКИНИ І СТІЙКІСТЬ ІНСУЛІНУ
Вісцеральні адипоцити виділяють жироспецифічні цитокіни, такі як лептин та адипонектин, а також запальні цитокіни, такі як фактор некрозу пухлини-α та інтерлейкін (ІЛ) -6. Недавні експерименти свідчать про те, що збільшення кількості жирової тканини, що стікає у ворітну вену, може спричинити резистентність до печінки та системної інсуліну [21▪]. У цьому дослідженні здатність жирової тканини, прищепленої до брижі, індукувати резистентність до інсуліну залежала від вироблення IL-6. Розмір вісцерального жирового депо та розмір адипоцитів у людини пов’язані із системною резистентністю до інсуліну, а також підвищеною експресією хемокінів та цитокінів імунними клітинами в тканині [22]. Недавнє дослідження також виявило кореляцію між підвищеною кількістю вісцерального жиру, гіпертрофією адипоцитів, резистентністю до інсуліну та підвищеною експресією генів аутофагії в жировій тканині людської сальникової тканини [23]. Ці результати дозволяють припустити, що схильність вісцеральної жирової тканини до посилення запалення та подальша секреція цитокінів, що погіршують інсулінову сигналізацію, може суттєво сприяти системній резистентності до інсуліну при центральному ожирінні.
НАДАННЯ ТА ЕКТОПИЧНЕ ВИКЛАДНЕННЯ ЛІПІДІВ ТА ІНСУЛІНОВА СТІЙКІСТЬ
Здатність зберігати калорії, що перевищують безпосередні енергетичні потреби, є біологічною адаптацією з великими еволюційними перевагами. Багато організмів, від глистів до ссавців, зберігають надлишок калорій у вигляді крапель тригліцеридів, які накопичуються в різних клітинах і типах тканин, таких як кишечник, жирове тіло та печінка [29,30]. Жирова тканина вперше з’являється в процесі еволюції, що оточує кишечник та внутрішні органи, можливо, служить для підтримки температури, оскільки останні дані свідчать про те, що жирова тканина, що оточує аорту, має коричневе жирове походження [31]. Це свідчить про те, що ці жирові склади виконують захисну та біомеханічну ролі. Утворення великих підшкірних жирових депо з'являється пізніше в процесі еволюції і є критичним для зберігання великої кількості жиру в періоди надлишку калорій.
РОЗШИРЕННЯ ТА ТКАНИН І ЗАХИСТ ВІД ІНСУЛІНОВОЇ ОПОРНОСТІ
Порушення здатності зберігати окремі жирові клітини призводить до ектопічного відкладення ліпідів у критично важливих органах, включаючи вісцеральну жирову тканину, печінку та м’язи [36]. Таким чином, критичним фактором захисту від резистентності до інсуліну є розширюваність жирової тканини, що визначається як здатність утворювати нові адипоцити, які можуть накопичувати надлишок енергії та захищати від гіпертрофії адипоцитів та накопичення ектопічних ліпідів. Механізми, що визначають розширюваність жирової тканини, невідомі, але, як і будь-яка зростаюча тканина, обов’язково беруть участь здатність реконструювати позаклітинний матрикс та адекватно збільшити васкуляризацію капілярів, щоб забезпечити надходження кисню та поживних речовин.
Кілька досліджень показали наявність гіпоксії в жировій тканині у людей, що страждають ожирінням [37,38 cross.tv], а нещодавній мікродіаліз підшкірної жирової клітковини черевної порожнини у людей показав, що ожиріння пов'язане з нижнім кровотоком жирової тканини [39 cross.tv], хоча докази гіпоксія в цьому дослідженні не виявлена. Гіпоксичний стрес в жировій тканині може призвести до аберантного перебудови позаклітинного матриксу, що призведе до фіброзу та запалення [40]. Таким чином, розширення капілярних мереж може бути важливим для запобігання гіпоксії, фіброзу та запалення при розширенні жирової тканини. Нещодавнє дослідження на пацієнтах із ожирінням, що страждають ожирінням, виявляє позитивну кореляцію між ангіогенною здатністю підшкірної клітковини та чутливістю до інсуліну, вказуючи на те, що недостатній ангіогенний ріст підшкірної жирової клітковини може відігравати певну роль у патогенезі метаболічних захворювань [41]. З'ясування факторів, що сприяють ангіогенному розширенню жирової тканини, є важливим напрямком майбутніх досліджень.
На підставі вищезазначених міркувань дуже важливо з’ясувати фактори, що визначають здатність особи розширювати підшкірну жирову тканину. Однією з можливостей, яку слід розглянути, є природні коливання кількості попередників адипоцитів. Ці клітини були ідентифіковані в строго-судинній фракції жирової тканини миші [42]. На початку розвитку такі фактори, як взаємодія матрикс-клітина та клітина-клітина, а також ангіогенез є важливими для диференціації адипоцитів від клітин-попередників [43]. Потрібна додаткова робота для подальшої характеристики властивостей цих клітин у специфічних складах жирової тканини у людини.
УСПІШНІ ТЕРАПЕВТИЧНІ СТРАТЕГІЇ ДОПОМОГАЮТЬ ЕЛІКІДАТНИХ МЕХАНІЗМІВ ІНСУЛІНОВОЇ ОПОРНОСТІ
Зміни у харчуванні є загальноприйнятими підходами до схуднення, і, хоча більшість спроб не приносять успіху через невідповідність пацієнта, все ще залишаються значні суперечки навколо найкращого дієтичного підходу. Недавній огляд кількох дієтичних втручань свідчить про те, що резистентні до інсуліну особи отримують найбільш короткочасну користь від дієти з низьким вмістом вуглеводів порівняно з дієтою з низьким вмістом жиру, ймовірно, через несприятливий вплив високого рівня вуглеводів на інсулін після їжі та рівні тригліцеридів [47]. Хоча показано, що обмеження калорій зменшує кількість жирових клітин у скелетних м’язах та самій вісцеральній жировій тканині, ці ефекти майже подвоюються, коли втрата ваги пов’язана з фізичними вправами у сидячих пацієнтів із надмірною вагою [48: 18]. Дослідження на гризунах дають механістичне уявлення про покращення інсулінорезистентності, пов’язане з фізичними вправами. Як гострі, так і хронічні фізичні навантаження на моделі ожиріння щурів, спричиненої дієтою, призводять до пригнічення сигналізації запалення в печінці, м’язах та жировій тканині, що згодом покращує передачу інсуліну [49].
ВИСНОВОК
Робота над з’ясуванням механізмів взаємозв’язку ожиріння та резистентності до інсуліну у людей продовжує підтримувати концепцію, згідно з якою вісцеральне ожиріння, але не підшкірне, призводить до інсулінорезистентності та підвищує ризик розвитку СД2. Механізми, за яких вісцеральне ожиріння призводить до резистентності до інсуліну, схоже, пов'язані з надлишковим накопиченням ліпідів у печінці. Це може бути пов’язано з надлишком жирних кислот з вісцеральної жирової тканини, що стікає у ворітну вену. Надмірне накопичення ліпідів може призвести до порушення сигналізації інсуліну через клітинні автономні механізми або через індукцію запалення та подальшу продукцію запальних цитокінів макрофагами, що погіршує дію інсуліну. Зберігання надлишку жиру в підшкірних депо зменшує ризик резистентності до інсуліну та T2DM, можливо, запобігаючи накопиченню жиру у вісцеральній жировій тканині, печінці та скелетних м’язах. Таким чином, механізми, що визначають розмір і розширюваність депо підшкірної жирової тканини, такі як контроль позаклітинного матриксу та розширення капілярів, можуть бути важливими цілями для майбутньої терапії.
КЛЮЧОВІ МОМЕНТИ
Вісцеральна жирова тканина збільшується, а підшкірна жирова тканина зменшує ризик інсулінорезистентності та T2DM у людей.
Ожиріння внутрішніх органів корелює із надлишковим накопиченням ліпідів у печінці.
Надмірне накопичення ліпідів може спричинити резистентність до інсуліну через клітинні автономні механізми, а також через індукцію запалення і, як наслідок, вироблення запальних цитокінів.
Неможливість розширення підшкірної жирової тканини паралельно з хронічним надлишковим споживанням калорій може бути наслідком порушення можливості розширення її позаклітинного матриксу та капілярної мережі, а також призвести до позаматкового накопичення ліпідів.
Подяки
Автори відзначають цінні дискусії з членами відповідних лабораторій та Центру діабету UMASS. Ми просимо вибачення за неможливість навести численні приклади важливої роботи в цій галузі через космічні міркування.
Виноски
Не існує конфлікту інтересів.
Конфлікт інтересів
Робота в лабораторіях авторів була підтримана грантами Національного інституту охорони здоров’я DK089101 для SC, DK30898 для MPC та Центру клінічної та поступальної науки UMASS для OTH.
ЛІТЕРАТУРА І РЕКОМЕНДОВАНЕ ЧИТАННЯ
Статті, що представляють особливий інтерес, опубліковані протягом річного періоду огляду, були виділені як:
▪ представляє особливий інтерес
▪▪ надзвичайний інтерес
Додаткові посилання, пов’язані з цією темою, також можна знайти в розділі «Поточна світова література» цього випуску (с. 142–143).
- Роль сечової кислоти в інсулінорезистентності у дітей та підлітків із ожирінням
- Що викликає інсулінорезистентні вилки над ножами
- Роль сечової кислоти в інсулінорезистентності у дітей та підлітків із ожирінням -
- Це поширене кулінарне масло викликає більше ожиріння та діабету, ніж цукор
- Дієта резистентності до інсуліну - огляд дієти