Кишкові коротколанцюгові жирні кислоти та їх зв’язок з дієтою та здоров’ям людини
Анотація
У товстій кишці живе щільна популяція мікроорганізмів, так звана «мікробіота кишечника», здатна ферментувати вуглеводи та білки, які уникають всмоктування в тонкому кишечнику під час травлення. Ця мікробіота виробляє широкий спектр метаболітів, включаючи коротколанцюгові жирні кислоти (SCFA). Ці сполуки всмоктуються у товстій кишці і визначаються як 1-6 вуглецевих летких жирних кислот, які можуть мати пряму або розгалужену ланцюгову конформацію. На їх виробництво впливає структура споживання їжі та опосередковані дієтою зміни мікробіоти кишечника. SCFA мають чіткі фізіологічні ефекти: вони сприяють формуванню кишкового середовища, впливають на фізіологію товстої кишки, вони можуть використовуватися як джерела енергії клітинами хазяїна та мікробіотою кишечника, а також вони беруть участь у різних механізмах передачі сигналів господаря. Ми узагальнюємо сучасні знання про вироблення SCFA, включаючи взаємодію перехресних годувань бактерій, та біологічні властивості цих метаболітів, що впливають на здоров’я людини.
Вступ
Мікробіота кишечника впливає на наше здоров’я та стадії харчування за допомогою безлічі механізмів, і все більша кількість доказів визнає, що мікробні метаболіти мають великий вплив на фізіологію господаря. Коротколанцюгові жирні кислоти (SCFA) - це леткі жирні кислоти, що виробляються мікробіотою кишечника у товстій кишці як продукти бродіння з харчових компонентів, які не всмоктуються/не засвоюються в тонкому кишечнику; вони характеризуються тим, що містять менше шести вуглеводнів, що існують у прямолінійній та розгалуженої ланцюговій конформації. Найбільш поширені оцтова кислота (С2), пропіонова кислота (С3) та масляна кислота (С4), що становить 90–95% SCFA, присутньої в товстій кишці. Основними джерелами SCFA є вуглеводи (CHO), але амінокислоти валін, лейцин та ізолейцин, отримані в результаті розщеплення білків, можуть перетворюватися в ізобутират, ізолевалерат та 2-метилбутират, відомі як SCFA з розгалуженими ланцюгами (BSCFA), мало (5%) до загального виробництва SCFA. Метою цього міні-огляду є узагальнення сучасних знань про вироблення SCFA, включаючи взаємодії бактеріальних схрещувань, та біологічні властивості цих метаболітів, що впливають на здоров'я людини.
Механізми виробництва SCFA
Метаболічні шляхи
Основними кінцевими продуктами, що виникають в результаті катаболізму СНО кишкових мікробів, є ацетат, пропіонат та бутират. Лактат, хоча і не є SCFA, також виробляється деякими членами мікробіоти, такими як молочнокислі бактерії, біфідобактерії та протеобактерії, але в нормальних фізіологічних умовах він не накопичується в товстій кишці через наявність деяких видів, таких як як Eubacterium hallii, який може перетворювати лактат у різні SCFA (Flint et al., 2015).
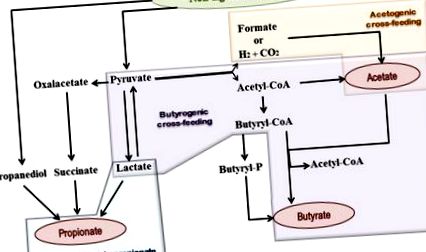
Ацетат є найпоширенішим SCFA в товстій кишці і становить більше половини загального SCFA, виявленого в калі (Louis et al., 2007). Описано два основні шляхи метаболізму для виробництва ацетату мікробіотою кишечника (рис. (Рис. 1). 1). Більшість ацетату виробляється більшістю кишкових бактерій в результаті ферментації СНО. Крім того, приблизно третина ацетату товстої кишки надходить від ацетогенних бактерій, які здатні синтезувати його з водню та вуглекислого газу або мурашиної кислоти шляхом Вуда-Люнгдала (Miller and Wolin, 1996; Louis et al., 2014 ).
Схематичне зображення мікробних метаболічних шляхів та механізмів перехресного годування, що сприяють утворенню SCFA в кишечнику людини. Затінені геометричні фігури узагальнюють шляхи утворення для кожного з трьох основних SCFA: ацетату, пропіонату та бутирату.
Метаболізм пропіонату та бутирату приділяли велику увагу протягом останніх років, головним чином, через зв’язок між низьким рівнем продуцентів бутирату та пропіонату бактерій та деякими захворюваннями, в яких беруть участь запальні процеси. Наприклад, у виробників бутирату зазвичай низький рівень виразкового коліту (Machiels et al., 2014), а у дітей із ризиком астми виявлено знижений рівень продуцентів пропіонату (Arrieta et al., 2015).
У бактерій, що продукують бутират, відомі два різні шляхи виробництва бутирату (рис. (Рис. 1). 1). Шлях бутират-кінази використовує ферменти фосфотрансбутирилази та бутират-кінази для перетворення бутирил-КоА в бутират (Louis et al., 2004). Цей шлях не є поширеним серед представників мікробіоти кишечника і в основному обмежується деякими видами копрококів (Flint et al., 2015). На відміну від цього, більшість виробників бутиратів кишечника (Louis et al., 2010), в тому числі, використовують шлях бутирил-КоА: ацетат КоА-трансферази, при якому бутирил-КоА перетворюється в бутират в одній стадії ферментативної реакції (Louis et al., 2010). деякі з найпоширеніших родів мікробіоти кишечника, такі як Faecalibacterium, Eubacterium та Roseburia. Примітно, що виробництво бутирату та пропіонату однією і тією ж бактерією не є поширеним явищем, і лише деякі анаероби, такі як Roseburia inulinivorans та Coprococcus catus, здатні продукувати і те, і інше (Louis et al., 2014).
Механізми перехресного годування
Перехресне годування бактеріями має величезний вплив на остаточний баланс виробництва SCFA та ефективну експлуатацію субстратів, що потрапляють в кишечник людини. Ці механізми полягають у використанні кінцевих продуктів із метаболізму даного мікроорганізму іншим, що називається метаболічним перехресним годуванням (рис. (Рис. 1), 1), та/або у використанні одним мікроорганізмом енергетично насиченого комплексу CHO продукти розпаду, утворені іншим, який називається перехресним подаванням субстрату (Belenguer et al., 2006; Flint et al., 2007). Нещодавнє дослідження silico показало, що взаємодії перехресного годування мутуалізму сприяли аноксичні стани, які частіше зустрічаються в товстій кишці, ніж у тонкій кишці (Heinken and Thiele, 2015).
Мікроорганізми, які не здатні використовувати складний СНО, можуть розмножуватися, використовуючи перевагу перехресного годування субстратом, використовуючи сполуки, що розщеплюються, продуковані гідролітичними бактеріями. Це стосується деяких видів Bifidobacterium, які не можуть використовувати фруктани інулінового типу (ITF), але можуть рости шляхом перехресного годування моно- та олігосахаридів, що виділяються первинними деградаторами інуліну в калових культурах, доданих з інуліном як джерелом вуглецю (Rossi et al., 2005; Salazar et al., 2009). Інший приклад - деградація агаро-олігосахаридів (АТ), яка є більш ефективною, коли Bacteroides uniformis та Escherichia coli вирощуються в спільних культурах, ніж у відокремленій монокультурі (Li et al., 2014). У цьому ж дослідженні автори пропонують використовувати агаротріозу, проміжний продукт у деградації АО, Bifidobacterium adolescentis та Bifidobacterium infantis. В іншій роботі було продемонстровано, що Roseburia sp. штам А2-183 не може використовувати лактат як джерело вуглецю, але коли його культивують з B. adolescentis L2-32 у присутності ФОС або крохмалю, утворюється бутират (Belenguer et al., 2006).
Вплив дієти на склад мікробіоти кишечника та вироблення SCFA
Таблиця 1
(A) Епідеміологічні дослідження, проведені з 2010 року, що показують вплив дієти на SCFA, що виробляється мікробіотою кишечника. Затінені ділянки вказують на зміну популяцій, що аналізуються, з точки зору їх стану здоров'я. D, дні; y, рік. (B) Інтервенційні дослідження, проведені з 2010 року, що показують вплив дієти на SCFA, що виробляється мікробіотою кишечника. Затінені ділянки вказують на зміну популяцій, що аналізуються, з точки зору їх стану здоров'я. D, день; ш, тиждень; м, місяць; y, рік.
Склад базальної мікробіоти також має глибокий вплив на кінцевий вплив, який діє in vitro дієтою на популяції мікробів та метаболічну активність (Arboleya et al., 2013a; Souza et al., 2014). У зв'язку з цим було виявлено різну реакцію на пробіотики та пребіотики з боку мікробіоти осіб з різних вікових груп (Arboleya et al., 2013a; Likotrafiti et al., 2014) або між людьми з ожирінням та худими (Yang et al., 2013).
Біологічні ефекти SCFA
Одним із наслідків для здоров’я, пов’язаного з виробництвом SCFA, є супутнє зниження просвіту рН, що саме по собі пригнічує патогенні мікроорганізми та збільшує поглинання деяких поживних речовин (Macfarlane and Macfarlane, 2012). Встановлено, що ацетат є ключовим фактором у здатності біфідобактерій інгібувати ентеропатогени (Fukuda et al., 2011). Більше того, бутират підживлює епітеліальні клітини кишечника та збільшує вироблення муцину, що може призвести до змін у адгезії бактерій (Jung et al., 2015) та поліпшення цілісності щільних з’єднань (Peng et al., 2009). Таким чином, виробництво SCFA, схоже, відіграє важливу роль у підтримці функції кишкового бар'єру.
Також було помічено, що SCFA захищає від розвитку колоректального раку (CRC), при цьому більшість досліджень зосереджуються на бутираті (Canani et al., 2011; Keku et al., 2015). Бутират сприяє рухливості товстої кишки, зменшує запалення, збільшує вісцеральне зрошення, індукує апоптоз і пригнічує прогресування клітин пухлини (Zhang et al., 2010; Canani et al., 2011; Leonel and Alvarez-Leite, 2012; Keku et al., 2015), всі ці властивості корисні для запобігання КПР. У ракових колоноцитах завдяки ефекту Варбурга накопичується бутират, який підвищує його активність як інгібітора деацетилювання гістонів, сприяючи апоптозу клітин CRC. Цікаво, що недавнє дослідження на тваринах свідчить, що захисна дія харчових волокон на КРК залежить від утворення бутирату мікробіотою (Donohoe et al., 2014).
Крім того, також повідомляється, що бутират і пропіонат індукують диференціювання Т-регуляторних клітин, допомагаючи контролювати запалення кишечника; здається, цей ефект опосередковується інгібуванням деацетилювання гістонів (Donohoe et al., 2014; Louis et al., 2014). Цей контроль запалення кишечника може бути корисним з точки зору підтримки кишкового бар’єру, зменшуючи ризик запальних захворювань кишечника або ХРН. На відміну від того, що відбувається з трьома основними кишковими SCFA, ацетатом, пропіонатом та бутиратом, мало відомо про потенційний вплив інших SCFA на здоров’я.
Заключні зауваження
Основна роль дієти полягає в забезпеченні достатньої кількості макро- та мікроелементів, щоб задовольнити щоденні потреби та добробут. Однак протягом останніх десятиліть зв'язок між споживанням їжі та фізіологією стає все більш визнаним, хоча багато молекулярні та імунологічні аспекти, за допомогою яких компоненти дієти можуть впливати на здоров'я людини, все ще залишаються невідомими. Бактеріальна ферментація CHO та білків виробляє SCFA, які стають головними посередниками у взаємозв'язку між харчуванням, мікробіотою кишечника, фізіологією та патологією. Багато біологічних ефектів, здається, опосередковуються цими бактеріальними метаболітами, але переконливих доказів немає для багатьох заяв щодо здоров'я, висунутих для SCFA. Були опубліковані перспективні дослідження in vitro та на тваринах, але їх неможливо легко екстраполювати на ситуацію з людиною. Слід вдосконалити підходи, що поєднують технології in vitro, in vivo та «omics», з акцентом на випробуваннях на втручанні людини, щоб дослідити механізми виробництва та дії SCFA, відкриваючи тим самим можливість знайти стратегії для розробки персоналізованих харчування.
Внески автора
Усі перелічені автори внесли значний, прямий та інтелектуальний внесок у роботу та схвалили її до публікації.
Заява про конфлікт інтересів
Автори заявляють, що дослідження проводилось за відсутності будь-яких комерційних або фінансових відносин, які можна трактувати як потенційний конфлікт інтересів. Рецензент BJ та редактор обробки заявили про свою спільну приналежність, а редактор обробки заявляє, що процес, тим не менше, відповідав стандартам чесного та об'єктивного огляду
Подяки
Ця робота фінансувалася проектом AGL2013-43770-R від Plan Nacional/Plan Estatal de I + D + I (Міністерство економіки та конкурентоспроможності Іспанії, MINECO). Діяльність групи пробіотиків та пребіотиків частково підтримується за допомогою гранту GRUPIN14-043 від “Регіонального плану розслідування делікатусів Астурії”. Як національні, так і регіональні гранти отримали співзасновники з фондів Європейського Союзу FEDER. ДР отримав докторантську стипендію FPI, тоді як НС отримує вигоду від докторського контракту Кларіна (Європейська програма Фонду Марії Кюрі), що співфінансується План регіонального розслідування принципадо Астурії, Іспанія.
- Геморой, як дієта може допомогти здоров’ю Охснера
- Харчування конопель, користь для здоров’я та дієта
- Ваш дієта робить вас депресивним Центром депресії - Повсякденне здоров'я
- Ліам Хемсворт каже, що його змусили припинити веганську дієту після того, як чоловіки налякають здоров'я; s Журнал «Здоров’я»
- Дієта та поради щодо лікування ішемічного коліту - Bel Marra Health