Лікування ожиріння та метаболічного синдрому трансплантацією калових мікробіоти
Кларисса А. Мароц
аспірантура з біомедичних наук, Каліфорнійський університет, Сан-Дієго, Ла-Холла, Каліфорнія
Амір Заррінпар
b Відділ гастроентерології Каліфорнійського університету, Сан-Дієго, Ла-Холла, Каліфорнія
Анотація
Поширеність метаболічного синдрому, який включає ожиріння та супутні захворювання, у всьому світі швидко зростає. Мікробіом кишечника людини визнаний незалежним екологічним модулятором метаболічного здоров'я та захворювань господаря. Дослідження на моделях на тваринах показали, що мікробіом кишечника має функціональну здатність індукувати або полегшувати метаболічний синдром. Одним із способів модифікувати мікробіом кишечника людини є трансплантація калових речовин, що містять велику кількість живих мікроорганізмів, від здорової особи до хворої в надії полегшити хворобу. Тут ми розглядаємо останні дані, що свідчать про ефективність трансплантації калових мікробіоти (FMT) у тваринних моделей та людей для лікування ожиріння та пов’язаних з ним метаболічних розладів.
Вступ
За останні півстоліття поширеність ожиріння та пов’язаних із цим метаболічних порушень, таких як діабет 2 типу (T2D), неалкогольна жирова хвороба печінки та гіперхолестеринемія, різко зросла. У сукупності ці захворювання спричиняють надмірне навантаження на витрати на охорону здоров'я та значну захворюваність та смертність. Хоча ці хвороби пов’язані з генетикою людини та зміною способу життя, мікробіом кишечника людини або мікроорганізми, що живуть у кишечнику та їх колективних геномах, зараз визнаний таким, що відіграє важливу роль у метаболічному здоров’ї та захворюваннях [1,2]. Трильйони різноманітних організмів, включаючи бактерії, гриби, археї та віруси, спільно еволюціонували, щоб жити в кишечнику людини [3]. Ці коменсальні організми складаються з мікробіома кишечника, а їх колективний геном, який називають метагеномом, містить понад стократну кількість генів, ніж їх господар [4]. Певні метагеномічні закономірності пов'язані з ожирінням, а також іншими фенотипами [5]. Ці закономірності реагують на зміну ваги у людей [6], що свідчить про те, що модуляція мікробіому кишечника динамічно корелює з метаболічним фенотипом людини-господаря.
Існує багато способів зміни мікробіоти кишечника, включаючи пробіотики (непатогенні організми, корисні для господаря), пребіотики (хімічні речовини, що індукують ріст та/або активність коменсальних організмів), а також трансплантацію мікробіоти калу (FMT) [7]. . Хоча в багатьох дослідженнях повідомлялося про корисні ефекти пробіотиків, жодне не свідчить про зміни у складі мікробіоти фекалій [8]. FMT, з іншого боку, спричиняє значні зміни у складі мікробіоти калу [9]. ФМТ як потенційний терапевтичний препарат має давню історію. Успішна практика зміни мікробіоти кишечника за допомогою ФМТ від здорової до хворої людини була вперше зареєстрована в 4 столітті для лікування важкої діареї [10]. Нещодавно рандомізовані контрольовані клінічні випробування показують вражаючі успіхи щодо повторної рефрактерної інфекції Clostridium dificile (CDI). Багато досліджень повідомляли про більш ніж 90-відсоткову ефективність, що суттєво успішніше, ніж традиційна терапія, у вирішенні повторних CDI [11]. Недавні дані, отримані на моделях на тваринах та людях, свідчать про те, що ФМТ також може бути використаний як терапевтичне втручання проти ожиріння [12,13]. У цьому огляді ми надамо оновлення стану ролі ФМТ у лікуванні ожиріння та пов’язаних з ним метаболічних розладів.
Кишкова мікробіота та метаболізм хоста
Тоді як міжособистісний склад мікробіоти може різко змінюватися, збережений набір профілів функціональних генів бактерій присутній у всіх здорових людей, що вказує на роль мікробіома у фізіологічному функціонуванні кишечника [1,14,15]. Зміни цієї складної фізіологічної бактеріальної популяції, пов’язані з негативними функціональними наслідками або захворюваннями, відомими як дисбіоз, можуть спричинити запалення низького рівня та змінений кишковий гомеостаз. Дисбіоз пов’язаний з різними захворюваннями, включаючи ожиріння та пов’язані з цим метаболічні порушення [16].
Методологія трансплантації фекальних речовин
В даний час FDA схвалює лише періодичні CDI для терапії FMT, не вимагаючи схвалення нового лікарського засобу (IND). Отже, більшість реципієнтів ФМТ отримували лікування від важкого ІРС. Ці особи не змогли повторити лікування антибіотиками, і у них залишилось небагато терапевтичних варіантів. Крім того, FMT вивчався при запальних захворюваннях кишечника (ВЗК), оскільки етіологія цього захворювання, принаймні частково, є наслідком дисбіозу. Однак контрольованих рандомізованих досліджень для пацієнтів із ВЗК було небагато, і немає жодних доказів того, що ФМТ покращує клінічні результати. Загалом, ФМТ проводився в основному хворим особам, які мають високий ризик ускладнень. Отже, потенційні ризики та ускладнення для відносно здорових пацієнтів із ожирінням або метаболічним синдромом залишаються гіпотетично нижчими порівняно з попередніми дослідженнями, проведеними у пацієнтів з рефрактерною, періодичною CDI або IBD.
Незважаючи на те, що FMT порівняно простий у виконанні, методологія має широкі міжінституційні мінливості. Наприклад, готуючись до ФМТ, деякі установи дають своїм пацієнтам багаторазові дози доксицикліну або ванкоміцину, намагаючись зменшити рідну, дисбіотичну популяцію [29]. У багатьох закладах, безпосередньо перед проведенням ФМТ, пацієнтам зазвичай дають препарат з поліетиленгліколю товстої кишки, щоб збільшити можливість для трансплантованого мікробіома успішно колонізувати кишечник, незалежно від того, вводиться ФМТ у верхні відділи шлунково-кишкового тракту або через колоноскопію. Однак опублікованих доказів того, що цей препарат покращує клінічні результати FMT, немає [22].
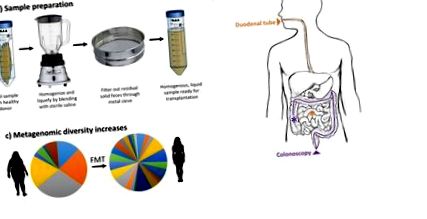
Обробка калових речовин для трансплантації не стандартизована, і для оптимальної ефективності її потрібно перевірити експериментально. Однак загальний принцип є більш-менш універсальним. Як зазначено на малюнку 1, донорський стілець спочатку змішують із сольовим розчином для гомогенізації його до рідкого зразка, а потім фільтрують для видалення твердих фекалій, які можуть заважати трансплантації. З метою стандартизації обробки калових речовин, дослідження порівнювали ефективність заморожених та свіжих зразків стільця до обробки та трансплантації. До цих пір ці дослідження не показали значної різниці у первинних результатах [30,31]. Хоча дослідження проводили секвенування 16РРНК до та після обробки для оцінки втрати зразків, фекальні речовини містять 99 відсотків анаеробних видів, які можуть не пережити енергійного аеробного змішування [32,33]. Крім того, секвенування 16РРНК не відрізняє життєздатність від мертвих клітин. Тим не менше, переважна кількість позитивних результатів, отриманих від FMT при лікуванні хворих на ІХС, свідчить про те, що або життєздатність клітин є відносно незначною, або що невелика частка вижилих клітин є достатньою, щоб викликати зміну мікробіома реципієнта та терапевтичний ефект.
Схема трансплантації калових мікробіоти. А) Фекальні речовини донора змішують із сольовим розчином та проштовхують через металеве сито для отримання однорідного рідкого розчину. Б) Оброблена калова мікробіота доставляється або через дванадцятипалу кишку, або за допомогою колоноскопії. В) Репрезентативні дані, що свідчать про метагеномне розмаїття, збільшуються після прийому ФМТ від худого донора до реципієнта із ожирінням.
Оброблені фекальні речовини, як правило, надходять у шлунково-кишковий тракт пацієнта за допомогою колоноскопії або дванадцятипалої кишки/верхньої ендоскопії (рис. 1B). Хоча шлях доставки часто варіюється від дослідження до дослідження, статистично значущої різниці в результатах між методами доставки для лікування CDI не повідомляється [11,34]. Цей висновок залишається підтвердженим для лікування інших захворювань, таких як ВЗК або ожиріння. Незважаючи на це, важливо враховувати потенційні ризики, пов'язані з кожним потенційним маршрутом доставки.
Протокол для FMT широко варіюється, як узагальнено в таблиці 1, і стандартизація цієї методики повинна допомогти з'ясувати ефективність FMT.
Таблиця 1
| Точки мінливості | Потенційна методологія | Потенційні наслідки |
| Підготовка пацієнта | Тип/тривалість лікування антибіотиками, тривалість препарату товстої кишки | Стан мікробіома кишечника пацієнта може вплинути на сприйнятливість до трансплантації |
| Донор | Родич пацієнта, «супердонор», дизайнерські культури? | Визначення «супердонорів» натякає на можливість рухатись до створення більш безпечних, більш стандартизованих синтетичних пробіотичних спільнот |
| Підготовка зразка | Аеробний проти анаеробного; свіжий проти заморожений проти ліофілізований | Нещодавнє клінічне дослідження не показало різниці в клінічній роздільній здатності між використанням свіжого або замороженого зразка калу для трансплантації |
| Адміністрація | Дуоденальна трубка, колоноскопія, клізма, таблетки | Максимізація практичності цієї методики при збереженні ефективності може вплинути на її призначення та вартість |
| Сайт доставки | Товста кишка, тонка кишка | Просторова динаміка людського мікробіома залишається погано охарактеризованою, але може призвести до більш цілеспрямованої терапії |
Чутливість до інсуліну передається від донорів реципієнтам
Недавні дослідження на моделях на тваринах показують функціональний зв’язок між мікробіомом кишечника та ожирінням та пов’язаними з цим метаболічними порушеннями. Наприклад, ожиріння та резистентність до інсуліну у дорослих щурів на дієті з високим вмістом фруктози було скасовано при застосуванні перорально антибіотиків або орального FMT від контрольних щурів [13]. Нещодавно було досліджено трансплантацію калових речовин з близнюків, що не відповідають ожирінню, безмікробним мишам [35]. Миші, заселені мікробіомом від ожиріння близнюків, мали підвищене ожиріння та зменшили різноманітність бактерій порівняно з мишами, заселеними мікробіомом із худих близнюків. Ці результати демонструють здатність мікробіома змінювати метаболічний фенотип господаря.
На сьогоднішній день було опубліковано лише одне дослідження, що перевіряє ефективність FMT спеціально для лікування метаболічних розладів у людей. Відмінною рисою метаболічного синдрому є резистентність до інсуліну, коли клітини гіпореагують на інсулін і тому не можуть підтримувати гомеостаз глюкози. Мікробіота калу від здорових, худих донорів, переданих через дванадцятипалу кишку, людям із ожирінням з діагнозом T2D впливає на метаболізм господаря [12]. У дослідженні порівнювали пацієнтів, які отримали алогенну трансплантацію (n = 9) (тобто кал у здорового донора), та аутологічну трансплантацію (n = 9) (тобто їх власний стілець). Хоча не було зафіксовано різниці в індексі маси тіла через шість тижнів після трансплантації, спостерігалося значне підвищення чутливості до інсуліну (як вимірюється середньою швидкістю зникнення глюкози) та різноманітності мікробіоти калу, а також зменшення SCFA в калі в алогенній та аутологічній групах . Ці багатообіцяючі результати широко цитувались та надихали на численні клінічні випробування (обговорювані нижче). Хоча FMT може спричинити зміну мікробіома щодо популяції донорів протягом 24 тижнів після FMT [29], необхідні подальші дослідження, щоб визначити, чи може FMT мати довгостроковий вплив на чутливість до інсуліну або вагу.
Необхідні додаткові клінічні випробування для підтвердження ефекту ФМТ у пацієнтів із ожирінням або метаболічним синдромом. Важливо, що ці дослідження повинні бути рандомізованими, включати аутологічний контроль, містити прискіпливі метадані та відстежувати довгострокові дані про мікробіом та результати пацієнта. ClinicalTrials.gov перелічує чотири поточні клінічні випробування, які тестують FMT для лікування метаболічного синдрому. Клінічне випробування фази 2 в Массачусетській лікарні загального користування оцінює вплив капсул FMT на первинний результат зменшення маси тіла протягом 18 тижнів [ClinicalTrials.gov ID> NCT02530385]. Клінічне дослідження італійської фази 3 відстежує гомеостаз глюкози протягом 6 місяців після прийому ФМТ у поєднанні з дієтою та фізичними вправами [ClinicalTrials.gov ID> NCT02050607]. Дослідники з Нанкінського медичного університету Китаю оцінюють результати клінічного випробування фази 3 на одному FMT, що доставляється з назогастралу на T2D, протягом дворічного періоду [ClinicalTrials.gov ID> NCT01790711]. Канадське подвійне сліпе пілотне дослідження тестує ефективність FMT як при метаболічному синдромі, так і при неалкогольній жировій хворобі печінки, яка тісно пов’язана з ожирінням [ClinicalTrials.gov ID> NCT02496390].
Результати цих клінічних випробувань повинні дати нам краще уявлення про функціональну роль мікробіома в метаболічному розладі людини. Подальші дослідження повинні бути розроблені для того, щоб визначити, які популяції бактерій або функціональні стосунки мікробів-господарів лежать в основі цього явища.
Супердонори
Вибір донора для FMT не стандартизований, хоча існує загальний консенсус щодо необхідності робити це [36]. Спочатку донорами, як правило, були члени сім'ї, яких ідентифікував пацієнт. Однак останні дослідження підкреслюють практичні переваги використання стандартизованих добровільних донорів та створення перевірених біобанків [31,34]. Загалом, донорів обстежують на здоровий випорожнення відповідно до таблиці калу в Брістолі, інфекційних захворювань, недавньої історії подорожей та історії антибіотиків.
У подальших публікаціях та конференціях Vrieze et al. відзначали, що пацієнти, які мали більш сильне поліпшення чутливості до інсуліну після ФМТ, отримували трансплантацію від такої ж обмеженої кількості донорів [37]. Тобто меншість зразків донорів викликали стійку реакцію, тоді як інші зразки не впливали на метаболізм пацієнтів. Отже, успіх втручання можна віднести до «супердонорів». Дослідження впливу FMT на полегшення симптомів ВЗК також виявили, що зразки калу певних донорів мають набагато більший терапевтичний ефект на кількох реципієнтів [38]. В даний час неможливо ідентифікувати супердонорів до початку експериментів. Більш пізні дослідження FMT намагаються ідентифікувати супердонорів раніше, щоб провести більш суворий аналіз їх мікробіому для ідентифікації терапевтичної мікробіоти, що може дозволити розробити кращу альтернативу FMT.
З FMT існує сильна соціальна стигма [39]. Оскільки фекальні речовини важко стандартизувати, етичні та соціальні ускладнення при пересадці фекалій та труднощі монетизації активно шукають альтернативи прямому ФМТ [40]. Гелеві капсули калової мікробіоти - нова перспективна методика, яка виключає необхідність проведення будь-яких шлунково-кишкових процедур [34,41] і є переважною для пацієнтів [42,43]. Насправді приватні компанії вже постачають FMT через оральні капсули, головним чином для лікування CDI. Однак незрозуміло, чи ефективні ці капсули, як сам ФМТ.
Іншим можливим методом лікування є розробка та виробництво пробіотиків незалежно від донорів. Наприклад, дослідження Vrieze та співавт. Виявили збільшення продукуючих бутират мікробів у пацієнтів із підвищеною чутливістю до інсуліну після FMT [8]. Якщо збільшення продукуючих бутират бактерій має важливе значення для поліпшення метаболічних симптомів, то існує можливість більш прямого лікування метаболічного синдрому за допомогою про/пребіотиків, які було б простіше контролювати та вводити.
Потенційні ризики
Однією із проблем FMT є складність у пошуку точних показників побічних реакцій. Наразі переважна більшість реципієнтів хворіють, і важко розрізнити нормальне прогресування захворювання та наслідки ФМТ. Тим не менше, хоча сотні людей перенесли ФМТ, мало негативних наслідків, навіть у пацієнтів із ослабленим імунітетом [44]. Більшість зафіксованих негативних симптомів є легкими, включаючи діарею або лихоманку [45-47]. Смертність спостерігалась у випробуваннях ФМТ, однак це було пов'язано з незв'язаними причинами у важкохворих або літніх пацієнтів. Мікробіота може схилити до сприйнятливості до атеросклерозу, використовуючи причинно-наслідкові докази у мишей та відповідні дані у людей [48]. Крім того, поширення трансмісивної хвороби, хоча і не повідомляється, все ще є життєздатною загрозою, особливо для людей з ослабленим імунітетом (наприклад, хворих на ВЗК на імуномодулюючій терапії, хворих на ВІЛ з CDI). Ці звіти підкреслюють важливість ретельного відбору донорів. Нарешті, ці ризики потрібно пом'якшити із урахуванням захворюваності та смертності, пов'язаних із ожирінням та пов'язаними з цим метаболічними захворюваннями, які на сьогодні мають мало ефективних методів лікування.
Дивно, але обезогенні властивості мікробіома кишечника можуть передаватися також через FMT. У звіті про ситуацію задокументовано передачу фенотипу ожиріння від донора із надмірною вагою до худого пацієнта після лікування ФМТ для лікування CDI [49]. Донором був молодий родич із ожирінням, який під час донорства швидко набирав вагу. Одержувачем була людина, яка ніколи не страждала ожирінням. Після прийому FMT у реципієнта спостерігався швидкий ненавмисний набір ваги, який не можна пояснити відновленням лише від CDI. Цікаво, що одержувач повідомив про підвищений апетит. Ці спостереження залишаються суперечливими, враховуючи те, що це повідомлення про справу. Однак це узгоджується з дослідженнями на гризунах, де перенесення калових речовин від ожирілих мишей до безмікробних мишей передає метаболічний фенотип [35]. Незважаючи на це, результати цього звіту вплинули на протокол FMT у багатьох установах, які зараз виключають донорів з ожирінням.
Висновок
FMT залишається захоплюючою терапією з великим потенціалом. Тим не менше, бракувало контрольованих, рандомізованих досліджень щодо метаболічних захворювань. Спочатку FDA вважала FMT IND, що ускладнювало практикуючим його використання, поки не були вичерпані всі інші терапевтичні можливості. Однак у 2014 році FDA заявила, що вона буде здійснювати розсуд щодо правозастосування, дозволяючи лікарям використовувати FMT без додатків IND для лікування CDI. Для отримання більш детальних показань FMT, як і раніше, необхідна заявка IND з FDA.
Враховуючи кількість контрольованих клінічних досліджень, які в даний час тестують ФМТ на метаболічний синдром, ми повинні мати чітке вказівку протягом наступних кількох років, чи є зміни мікробіоти причинними чи корелятивними у цій зростаючій епідемії, і чи змінюють мікробіом кишечника за допомогою ФМТ або подібних процедур забезпечить нові терапевтичні варіанти ожиріння та пов’язаних з ним метаболічних розладів.
- Вплив кленового сиропу на різноманітність мікробіоти кишечника та метаболічний синдром - Повний текст
- Трансплантація калових мікробіоти при лікуванні ожиріння - клінічний радник
- Трансплантація калу для лікування ожиріння та діабету MedPage сьогодні
- Вплив індукованого флеботомією запасів заліза в організмі на метаболічний синдром виникає внаслідок
- Центр метаболізму та схуднення «Столичне здоров’я»; Покриття ожиріння