Безпека Canephron® N для лікування інфекцій сечовивідних шляхів у першому триместрі вагітності
Анотація
Передумови
Інфекції сечовивідних шляхів (ІМП) є одними з найбільш часто зустрічаються бактеріальних інфекцій, особливо у вагітних. Канефрон® N (Bionorica, Німеччина) - це фітотерапевтичний лікарський засіб, що надає плейотрофний вплив на сечовидільну систему, включаючи сечогінну, спазмолітичну, протизапальну, протимікробну та нефропротекторну дію. Метою цього ретроспективного дослідження була оцінка безпеки Canephron® N при застосуванні у першому триместрі вагітності для лікування ІМП.
Методи
Це було ретроспективне багатоцентрове дослідження, яке оцінювало вплив Canephron® N у 384 жінок, які застосовували рослинні препарати протягом першого триместру вагітності (між 2004 і 2009 роками), і вагітність яких закінчилася живонародженими. Кінцевими точками, оціненими в цьому дослідженні, були наявність вроджених вад у новонародженого.
Результати
Не було значних відмінностей у частоті вроджених вад розвитку у новонароджених, матері яких приймали Канефрон® N у першому триместрі вагітності, порівняно з національними статистичними даними щодо населення Києва за той самий період. Більшість новонароджених (> 65%), матері яких отримували Canephron® N протягом першого триместру вагітності, мали показники Апгар 8 і вище, що свідчить про відмінний статус безпеки.
Висновки
Результати нашого дослідження вказують на те, що застосування Canephron® N протягом першого триместру вагітності не асоціювалось з будь-якими тератогенними, ембріотоксичними чи фетотоксичними ефектами на плід.
Передумови
Інфекції сечовивідних шляхів (ІМП) є одними з найбільш часто зустрічаються бактеріальних інфекцій, особливо у вагітних. Вагітність пов'язана зі специфічними фізіологічними, структурними та функціональними змінами сечовивідних шляхів, які сприяють росту бактерій та висхідним інфекціям [1]. Під час вагітності від 5 до 10% жінок страждають ІМП, як правило, безсимптомною бактеріурією, гострим циститом та пієлонефритом [2]. Більшість ІМП спричинені бактеріальними видами кишково-кишкового походження, а саме Кишкова паличка, що становить 70–85% випадків [3], а також Klebsiella pneumoniae, Золотистий стафілокок та стрептококи групи В [4–6]. Якщо їх не лікувати належним чином, ці інфекції можуть мати серйозні наслідки для матері та плоду, збільшуючи ризик прееклампсії, передчасних пологів та низької ваги новонароджених [1].
Антибіотики часто призначають для лікування ІМП у вагітних. Через зміну фармакокінетики лікарських засобів під час вагітності та можливість перенесення препарату через плацентарний бар’єр до застосування антибіотиків під час вагітності слід підходити з обережністю [7, 8]. Через потенційний тератогенний ефект певні антибіотики непридатні для використання у вагітних [9]. Антимікробні засоби, які вважаються безпечними під час вагітності, відносяться до класу β-лактаму, включаючи пеніциліни, цефалоспорини та фосфоміцин трометамол [6, 10]. Тим не менше, застосування антибіотиків загалом пов'язане з побічними явищами, включаючи алергічні реакції, побічні ефекти з боку шлунково-кишкового тракту та аритмію серця [11, 12], і їх слід вводити з максимальною обережністю під час вагітності. Крім того, кількість антимікробних засобів, безпечних для використання під час вагітності, додатково обмежується появою стійкості до ліків серед різних видів бактерій [6, 13]. Таким чином, існує потреба в альтернативних способах лікування для лікування ІМП, які виникають під час вагітності.
Canephron® N (Bionorica, Німеччина) - це фітотерапевтичний лікарський засіб, що складається з фіксованої комбінації трави столітника (Кентаврій sp.), корінь любистку (Levisticum officinale Кох) та листя розмарину (Rosmarinus officinalis Л.). Встановлено, що рослинні компоненти, що містяться у препараті, мають плейотрофний вплив на сечовидільну систему, включаючи діуретичний [14, 15], спазмолітичний [16, 17], протизапальний [18–20], протимікробний [21–24] та нефропротекторні ефекти [25]. Клінічні дані виявили терапевтичну користь для пацієнтів з ІМП, нефролітіазом або сечокам’яною хворобою [26, 27]. Канефрон® N доступний на європейському ринку понад 40 років і зареєстрований як традиційне рослинне ліки, але в даний час не ліцензований для використання під час вагітності та годування груддю. Однак за межами Європейського Союзу (ЄС) це одне з найбільш часто призначаються фітотерапевтичних препаратів для вагітних для лікування верхніх і нижніх ІМП. Хоча клінічні дослідження на вагітних показали, що Canephron® N безпечний і добре переноситься, до цих пір жодні дослідження не зосереджувались конкретно на аспектах його безпеки при застосуванні протягом першого триместру вагітності.
Метою цього ретроспективного дослідження була оцінка безпеки Canephron® N при застосуванні у першому триместрі вагітності для лікування ІМП. Основною кінцевою точкою цього дослідження була наявність вроджених вад у новонародженого.
Методи
Вивчати дизайн
Це було ретроспективне багатоцентрове дослідження, яке оцінювало вплив Canephron® N у 384 жінок, які застосовували рослинні препарати протягом першого триместру вагітності, і вагітність яких закінчилася живонародженими. Усі жінки проходили спостереження до кінця вагітності в клініці акушерства та гінекології Isida, Інститут педіатрії, акушерства та гінекології УАМН, з 2004 по 2009 рр. Усі пацієнти надавали письмову інформовану згоду щодо використання їх дані для цілей дослідження. Дані у національному реєстрі подаються лише як частота (у% від деформацій) у робочих документах. Тому неможливо надати точну кількість контрольних пацієнтів. Незважаючи на це, дані перевіряються та передаються у національний реєстр.
Вивчіть популяцію та лікування Canephron® N
Оскільки, як відомо, паритетний статус особи суттєво впливає на результат вагітності [28], а кількість різнопланових випадків виявилася недостатньою для окремого дослідження, ми включили в нашу оцінку первісток (одноплодних) та багатопородних випадків. Всі учасники повинні були приймати Canephron® N протягом щонайменше 14 днів протягом першого триместру вагітності для лікування ІМП. Добова доза Canephron® N становила 6 таблеток або 150 крапель. У більшості випадків жінки приймали Canephron® N, перш ніж дізнатися про свою вагітність. Основними критеріями виключення були наявність спадкових захворювань, багатоплідна вагітність та хронічний вплив відомих токсичних або генотоксичних речовин.
Кінцеві точки
Основною кінцевою точкою цього дослідження була наявність вроджених вад у новонародженого. Крім того, внутрішньоутробні вади розвитку оцінювали відповідно до Міжнародної класифікації хвороб (МКБ) -10 Всесвітньої організації охорони здоров’я (ВООЗ) [29]. Зокрема, оцінювали наявність вроджених вад розвитку статевих органів, вроджених вад розвитку сечовидільної системи, вроджених вад розвитку та деформацій опорно-рухового апарату та інших вроджених вад розвитку [29]. Отримані результати порівнювали з національними статистичними даними для Києва за той самий 5-річний період від первісткової вагітності у жінок, які не застосовували Canephron® N. Статус новонародженого немовляти оцінювали за 10-бальною системою балів за шкалою Апгар за одну хвилину після народження [30].
У разі наявності патологічного розладу вагітності та/або розвитку у новонародженого проводили подальші оцінки, щоб оцінити взаємозв'язок між вадами розвитку та прийомом Канефрона N® (включаючи тривалість прийому препарату, прийом інших ліків, вік матері, наявність дефектів у сім'ї, лабораторні дані, вплив інших відомих факторів ризику, таких як куріння або деякі професійні небезпеки). Наявність вроджених вад розвитку у немовляти оцінювали поряд із часом, коли мати приймала Канефрон® N (використовуючи перший день останньої менструації як орієнтир).
Статистичний аналіз
Статистичний аналіз результатів проводили за допомогою статистики для Windows® (версія 5.3, Statsoft, США). Коефіцієнти відносного ризику (RR) розраховували за наступними формулами:
Де RR = відносний ризик, стор 1 = частота події в експериментальній групі, і стор 2 = частота події в контрольній групі.
де SE = стандартнапомилка 0,05,
р 1 і р 2 = кількість подій в експериментальній та контрольній групах,
n 1 і n 2 = кількість пацієнтів в експериментальній та контрольній групах,
95% довірчий інтервал ДІ = loge RR ± 1,96 × SM.
Результати
Вік учасників коливався від 17 до 39 років (у середньому 21 ± 2,2 року). Загалом 170 (44,3%) жінок були первістками та 214 (55,7%) - багатопородними. З 384 жінок 361 приймали таблетки Canephron® N (6 таблеток щодня), а 23 отримували краплі Canephron® N (150 крапель щодня). Середня тривалість лікування становила 23 ± 1,25 дня. У 196 випадках (51,05%) Canephron® N застосовували як монотерапію, а у 188 випадках (48,95%) - як частину комбінованої терапії (поряд з антибактеріальними засобами фосфоміцином, амінопеніцилінами та цефалоспоринами). Показання до лікування Canephron® N у досліджуваній популяції зведені в таблицю 1.
Не було суттєвих відмінностей у частоті вад розвитку у новонароджених, матері яких приймали Канефрон® N у першому триместрі вагітності, порівняно з національними статистичними даними щодо населення Києва за той самий період 2004–2010 рр. (Табл. 2). З 384 жінок, які приймали Canephron® N протягом першого триместру вагітності, загалом 14 (3,65%) народили дітей з вродженими вадами розвитку. Цей відсоток подібний до показника серед населення Києва в цей період (3,71% за даними звіту Державної установи «Центр статистики охорони здоров’я МОЗ України».
У популяції Canephron® N було два випадки вад розвитку сечовидільної системи (обидва ниркові агенезиси). Був один випадок дублювання тазової системи та один випадок позаматкової тазової нирки. Серцеві вади розвитку включали транспонування великих артерій, дефект міжпередсердної перегородки та аномалію Ебштейна. Пороки розвитку нервової системи включали агенезію мозолистого тіла, кісту головного мозку та вроджену гідроцефалію з шлуночковою мегалією. Пороки розвитку травної системи складалися з анальної атрезії та пілоростенозу. Пороки розвитку опорно-рухового апарату включають відсутність дистальної фаланги пальця та синдактилії стопи.
Далі ми розглянули взаємозв'язок між термінами введення Канефрон® N у першому триместрі вагітності та наявністю будь-яких вроджених вад розвитку у новонародженого (табл. 3). Термін прийому Canephron® N оцінювали щодо першого дня останньої менструації.
З 4 жінок, які приймали Canephron® N у найраніший та найуразливіший період вагітності (29–50 день), жодна з їх немовлят не мала вроджених вад розвитку. З 106 жінок, які приймали Canephron® N між 51–70-м днем, 4 народили немовлят із вродженими вадами розвитку, а 10 із 274 жінок, які приймали Canephron® N між 71–84-м днем, народили дітей з вродженими вадами розвитку. Частота цих вад розвитку подібна до загальної кількості населення Києва.
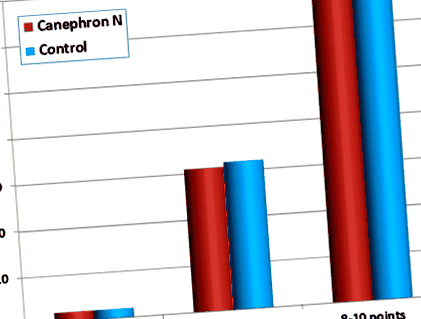
Ми розрахували RR та 95% довірчий інтервал (ДІ) розвитку вроджених вроджених вад у новонароджених, матері яких приймали Canephron® N у першому триместрі вагітності. RR становив 0,941 (95% ДІ: 0,526–1,68), що вказує на відсутність будь-якого впливу Canephron® N на частоту вроджених вроджених вад у нашому дослідженні. Нарешті, статус новонароджених оцінювали через одну хвилину після народження за допомогою бальної системи Апгар (рис. 1). Використовуючи бальну систему Апгар, кожній з п’яти основних характеристик (частота серцевих скорочень, дихальні зусилля, м’язовий тонус, рефлекторна дратівливість та колір) присвоюється значення від 0 до 2. Загальний бал - це сума п’яти підбалів, оцінка 7 і більше, що вказує на те, що стан новонародженої дитини хороший до відмінний [30]. Більшість новонароджених мали оцінки 8–10 балів за шкалою Апгара, що свідчить про те, що їх стан був чудовим, і свідчить про те, що застосування Канефрона® N протягом першого триместру вагітності не впливало на загальний стан новонароджених.
Десятки новонароджених Апгар, матері яких застосовували Канефрон® N протягом першого триместру вагітності. Червоний: Новонароджені пацієнтки, які отримували Канефрон® N у першому триместрі вагітності. Синій: Статистичні дані новонароджених з тих самих клінік, матері яких не приймали Canephron® N
Обговорення
Запальні захворювання сечовидільної системи є одними з найпоширеніших захворювань у вагітних [31]. Через гормональне розширення ниркової миски та сечоводів вагітні жінки мають підвищений ризик бактеріальної інвазії нирок та пієлонефриту [31]. Під час вагітності бактеріурія, яка переростає в пієлонефрит, була пов’язана з поганими наслідками для матері та дитини. ІМП під час вагітності збільшують ризик материнської гіпертонії, анемії та передчасних пологів, а також низької ваги при народженні [32, 33]. Тому вирішення ІМП, які виникають під час вагітності, є важливим засобом запобігання ускладненням вагітності.
Результати нашого дослідження щодо безпеки підтверджують раніше опубліковані висновки щодо Canephron® N у профілактиці та лікуванні ІМП та супутніх захворювань у вагітних. Три дослідження досліджували вплив Canephron® N на вагітних жінок, приділяючи головну увагу ефективності [35–37]. Дослідження Орджонікідзе та ін. включали 300 вагітних із низкою сечових патологій, включаючи безсимптомну бактеріурію, гестацію, загострення хронічного пієлонефриту або хронічне захворювання сечі без загострень [36]. Незалежне дослідження Medved та співавт. включали 30 вагітних із цукровим діабетом I типу, які мали гестаційний пієлонефрит або загострення хронічного пієлонефриту [35]. Третім дослідженням було проспективне рандомізоване дослідження, в яке було включено 85 вагітних із низкою патологій нирок [38]. У всіх трьох дослідженнях Canephron® N вводився поряд із стандартною терапією і мав сприятливий ефект у вагітних, які страждають на різні патології нирок. Хоча в цих дослідженнях не проводили детальних аналізів безпеки, Canephron® N продемонстрував хороший профіль безпеки та переносимості у всіх досліджуваних групах [27]. Слід зазначити, що препарат не вводили у першому триместрі вагітності у всіх трьох дослідженнях.
Два додаткові дослідження досліджували потенційний вплив Canephron® N на частоту вроджених вад розвитку [38, 39]. Репіна та ін. спостерігали 115 дітей (віком від 5 місяців до 3,5 років), народжених у жінок, які отримували лікування Канефроном® N протягом другого або третього триместру вагітності. Дослідження не повідомляло про негативні наслідки для плода під час вагітності та про відсутність наслідків після пологів на дітей, народжених від матерів, які проходили лікування препаратом під час вагітності [39]. Велике проспективно-ретроспективне дослідження, що оцінювало тератогенні, ембріотоксичні та фетотоксичні ефекти Canephron® N у 1647 жінок, не показало жодних доказів будь-яких наслідків для розвитку чи вроджених наслідків [38]. Наші дані ґрунтуються на результатах цих досліджень, припускаючи, що застосування Canephron® N протягом першого триместру вагітності не пов’язане з тератогенними ефектами на плід.
Обмеження нашого дослідження пов'язані з його ретроспективним дизайном і наслідком цього є відсутність даних про потенційні незрозумілі фактори, які могли вплинути на частоту вроджених вроджених вад у нашій досліджуваній популяції. Крім того, кількість осіб, включених до досліджуваної популяції, була відносно невеликою (загалом 384), і в (48,95%) випадках Канефрон N використовувався як частина комбінованої терапії (поряд з антибактеріальними засобами фосфоміцином, амінопеніцилінами та цефалоспоринами) . Варто також зазначити, що деякі користувачі могли переживати викидень через правило "все або нічого" на початку вагітності, і про такі випадки не повідомляється в цьому дослідженні.
Висновки
Результати нашого дослідження вказують на те, що застосування Canephron® N протягом першого триместру вагітності не асоціювалось з будь-якими тератогенними ефектами на плід і не впливало на загальний стан новонароджених.
- Симптоми, лікування та профілактика інфекцій мікоплазми
- Хірургічний аборт (перший триместр) Умови та лікування Здоров’я UCSF
- Безпека First Nestle India, австралійські продукти без глютену, фальсифікований індійський мед та багато іншого
- Вправи для вагітності перший триместр
- Прибивання фактів Безпека лікування нігтів під час вагітності - MotherToBaby