Зв’язок між дієтою та активністю хвороби у хворих на виразковий коліт з використанням нового методу аналізу даних
Анотація
Передумови
Повторюваний характер та різне географічне розповсюдження виразкового коліту (UC) впливає на фактори навколишнього середовища, такі як дієта, в його етіології.
Методи
Для того, щоб визначити, які продукти харчування можуть бути пов’язані з діяльністю хвороби в UC, був розроблений і застосований новий метод дієтичного аналізу. Вісімдесят один пацієнт з УК був прийнятий на роботу на всіх стадіях процесу захворювання. Після заповнення 7-денного щоденника дієти була проведена клінічна оцінка, що включала сигмоїдоскопічне обстеження (шкала від 0 (нормальна слизова) до 6 (дуже активне захворювання)). Вага їжі для кожної людини коригувався (ділився) на калорійність споживання людини за тиждень. Кожній споживаній їжі присвоювали бал сигмоїдоскопії (FSS), розрахований шляхом підсумовування продуктів (скоригованої) ваги споживаної їжі та балів сигмоїдоскопії для кожного пацієнта та наявності їжі та ділення на загальну (скориговану) масу споживаної їжі. всі 81 пацієнт. Таким чином, їжа, яку їдять у великих кількостях пацієнти з дуже активними захворюваннями, має високий рівень FSS і навпаки. Їжа, яку споживає
Передумови
Виразковий коліт (UC) - це хронічний, рецидивуючий розлад слизової, який безперервно поширюється проксимально від прямої кишки і обмежується товстою кишкою. Етіологія UC включає генетичний компонент, який, можливо, включає аномальну клітинну імунну відповідь на коменсальні кишкові бактерії в товстій кишці. Характер рецидиву/ремісії розладу та субстратний характер мікробного метаболізму у товстій кишці впливають на фактори навколишнього середовища, такі як дієта.
Окрім повноцінного харчування, дієтичні заходи не відіграють ролі в управлінні UC. Тим не менше, спроби пов'язати причину UC з конкретними продуктами харчування датуються щонайменше 50 роками [1]. Багато продуктів харчування або групи продуктів харчування пов'язані з UC (таблиця 1 - див. Додатковий файл 1) [2–13], включаючи цукор, яйця, безалкогольні напої, фрукти та овочі, білки, вуглеводи та жири. Однак жодне з них не має суттєвої користі або не сприяє справі UC. Частково це може бути тому, що важко виміряти як оцінку активності хвороби в UC, так і споживання їжі, або тому, що фактична дієтична складова, яка є ключовою для цього взаємозв'язку, не була виміряна.
Вважається, що сульфід, що утворюється в товстій кишці внаслідок бродіння амінокислот або відновлення сульфату, може бути пусковим фактором запального процесу ХК [14–16]. Нещодавно в проспективному дієтичному дослідженні, в якому кількісно визначали продукти, багаті сполуками сірки, було виявлено докази того, що сполуки сірки можуть збільшити ймовірність подальшого рецидиву UC [17].
Основним джерелом неорганічної сірки, переважно сульфату, в їжі є добавки сімейства S (IV); сульфітуючі агенти. Сульфіти використовуються як харчові консерванти з 17 століття і є одними з найбільш широко прийнятих та універсальних добавок. Сульфітуючі агенти, позначені в Європі E220–228 і загальновизнані як безпечні (GRAS) речовини в США, включають діоксид сірки, сульфіти водню, сульфіти та метабісульфіти. Сульфітуючі агенти дешеві, прості у використанні та надзвичайно ефективні для запобігання росту мікробів та зменшення псування [18]. Вони служать антиоксидантами, пригнічують ферментативні та неферментативні реакції підрум'янення та діють як модифікатор текстури бісквітного тіста. Сульфіти покращують вилучення кольору та стабілізацію виноградного сусла у виноробстві та захищають омарів та креветок від знебарвлення під час зберігання в льодах.
Однак існують певні проблеми із застосуванням сульфітів [19, 20]. На початку 1980-х років було виявлено, що прийом всередину або вдихання сульфітів спричинює бронхоспазм приблизно у 5% астматиків. Сульфітна чутливість може становити особливу загрозу на робочому місці, де використовуються сульфідуючі речовини, але може також виникати при попаданні в організм сульфітованих продуктів, таких як картопляні продукти та вино. Крім того, повідомлялося про чутливість шкіри, і існують анти-харчові ефекти, особливо для тіаміну, який легко розщеплюється сульфіт-іоном [21]. Механізм включає початкову нуклеофільну атаку на метиленовий вуглець, що активується позитивним зарядом на азоті, швидкість реакції досягає піку між рН 5 і 6 [18]. В результаті цього анти-харчового ефекту в США було переглянуто статус GRAS для сульфітів, і в 1986 р. Використання сульфітів у свіжих та заморожених фруктах та овочах було скасовано, а на етикетці потрібна декларація [22, 23]. Раніше (в США) їх вживання в м’ясі було заборонено, оскільки ці продукти є важливим джерелом тіаміну.
Тому було проведено дослідження дієти та активності захворювань в UC із використанням 7-денного дієтичного щоденника, повної оцінки активності захворювання та методу аналізу дієтичних даних, що дозволяє не помітити тенденції споживання їжі за допомогою звичного дієтичного програмного забезпечення.
Методи
Предмети
Набрано вісімдесят одного пацієнта, який перебуває в УК, і отримано поінформовану згоду. Етичний дозвіл надано Комітетом з медичної етики Тейсайду, Данді, Великобританія (посилання 007/00). Оскільки важливо мати широкий спектр захворювань, рекрутинг включав пацієнтів на всіх стадіях захворювання. Пацієнтів виключали, якщо клінічне обстеження або гістологія вказували на хворобу Крона або невизначений коліт, якщо позитивний посів калу на патогени або якщо пацієнт проходив лікування антибіотиками протягом 3 місяців до початку дослідження.
Дієтична оцінка
Усім хворим на УК було запропоновано заповнити 7-денний щоденник дієти [24]. Щоденник дієти був затверджений для використання в Європейському дослідженні перспективних досліджень раку (EPIC). Після заповнення дієтичного щоденника випробовувані відвідували дослідницьку клініку та проводили повну клінічну оцінку (див. Нижче). Інтервал часу між першим днем щоденника та клінічним візитом становив у середньому 28 днів. Таким чином, дієтичні дані є перспективними.
7-й щоденник дієти кодували та аналізували, використовуючи програмне забезпечення для аналізу поживних речовин Tinuviel, WISP v3.0 (Warrington, UK). Через різницю в протоколах сульфітування та широке використання сульфітуючих речовин, поточні таблиці складу харчових продуктів не містять неорганічних показників сірки і не можуть використовуватися для кількісної оцінки споживання. Замість кількісного споживання певних харчових компонентів, харчові продукти та групи продуктів харчування оцінювали в повному обсязі, використовуючи метод, описаний у розділі аналізу дієтичних даних (нижче).
Клінічна оцінка
Клінічна оцінка включала анамнез, фізичний огляд та загальну клінічну оцінку, а також повний аналіз крові, тести функції печінки та запальні маркери. Пацієнтів обстежували за допомогою жорсткої сигмоїдоскопії або флексісигмоїдоскопії та оцінювали за шкалою 0–6 (використовували цілі та напівцілі) відповідно до макроскопічних проявів слизової прямої кишки на відстані 5–10 см від анального краю [25]. Клінічна оцінка активності захворювання в кожному випадку підтверджувалась гістологічним дослідженням, проведеним одиноким гістопатологом, засліпленим до клінічних деталей, біоптацією прямої кишки, взятою із задньої стінки прямої кишки на 5–10 см від анального краю [26]. Простий клінічний показник коліту призначався пацієнтам під час кожного візиту за системою балів Уолмслі [27], разом із параметрами крові тяжкості захворювання (Hb, в'язкість плазми, СРБ, сироватковий альбумін).
Аналіз дієтичних даних
Закономірності прийому їжі, пов’язані з активністю захворювання, стали очевидними завдяки вивченню дієтичних щоденників, наприклад високе споживання сульфітосодержащих продуктів у поєднанні з сучасною обробленою, зручною дієтою було пов'язано з високим показником сигмоїдоскопії. Традиційне дієтичне кодування (WISP) не продемонструвало жодної такої чіткої взаємозв'язку між споживанням мікро- та макроелементів та оцінкою сигмоїдоскопії. Тому вважали, що традиційний дієтичний аналіз не містить важливих закономірностей у даних про дієту, і згодом був розроблений новий метод оцінки дієти.
Цей новий метод використовував наступну процедуру. Щоб розрахувати зв'язок певної їжі з клінічним балом, кожній їжі або спожитій групі продуктів харчування присвоювали бал сигмоїдоскопії (FSS), розрахований шляхом підсумовування продуктів ваги їжі та балів сигмоїдоскопії для кожного випадку їжі або групи продуктів харчування та ділення на загальна вага їжі або групи продуктів харчування, що міститься у всіх щоденниках. Для того, щоб кожен щоденник міг робити однаковий внесок у ФСС, вага кожної їжі регулювалася з використанням калорійності споживання для кожної людини. Цю процедуру проводили окремо для кожного продукту харчування, записаного в 7-му щоденнику дієт, але пояснюється нижче на прикладі червоного вина.
Оцінка червоного вина = (Σv (i) s (i))/Σv (i) для i = 1 до 81 рівняння 1.
i - 7-денний номер дієтичного щоденника (n = 81).
v (i) - обсяг (поділений на споживання калорій для пацієнта (i) червоного вина, записаного в 7-денному дієтичному щоденнику i.
s (i) - показник сигмоїдоскопії, пов’язаний із 7-денним дієтичним щоденником (i).
Таким чином, їжа, яку їдять у великих кількостях пацієнти з високим рівнем активності захворювання, матиме високі бали і навпаки. Знаменником у наведеному вище рівнянні є загальний обсяг їжі, про яку йде мова з усіх щоденників (з поправкою на споживання калорій), тому показники їжі можна прирівняти до впливу типової порції їжі, про яку йде мова, на бали сигмоїдоскопії пацієнтів . Ця процедура повторюється для кожного продукту харчування. Продукти харчування або групи продуктів харчування були виключені з аналізу, якщо 10 або менше людей їх споживали або якщо вони складали менше 1 кг від загального споживання всієї популяції. Рішення щодо того, де пролягають межі групи продуктів харчування, було прийнято залежно від чисельності групи та чи вважалися відмінності між продуктами харчування важливими для цього дослідження.
Статистика та обробка даних
Дієтичні дані були експортовані з WISP до Microsoft EXCEL 98 (версія Macintosh, 1998). Робочий аркуш, що містить основні заголовки; Ідентифікатор пацієнта, опис їжі, вага та оцінка сигмоїдоскопії пацієнта були заповнені. Далі дані сортували за описом їжі, а кожну їжу копіювали в окремий файл EXCEL. Потім рівняння 1 використовували для обчислення балів сигмоїдоскопії харчових продуктів для кожного продукту способом, подібним до прикладу в таблиці 2 (див. Додатковий файл 2).
Значення кореляції для графіків розсіювання були отримані за допомогою функції лінійної регресії в EXCEL. Рівняння t = r √ ((n-2)/(1-r 2)) у поєднанні з t таблицями забезпечило відповідні рівні значущості.
Результати
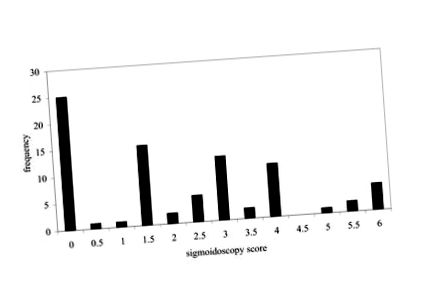
З 81 набраних пацієнтів 43 були чоловіки та 38 жінок. Середній вік (діапазон) чоловіків та жінок становив відповідно 53 (26–78) років та 47 (19–74 років). Розподіл балів сигмоїдоскопії показано на рис. 1. Третина пацієнтів мала показники сигмоїдоскопії 0, 0,5 або 1. Середній бал сигмоїдоскопії для всіх 81 пацієнта становив 2,09. Кореляція між показниками клінічної активності та показниками сигмоїдоскопії становила r 2 = 0,25 (n = 81).
Розподіл частоти балів сигмоїдоскопії (n = 81) для хворих на виразковий коліт, набраних на всіх стадіях захворювання.
У таблиці 3 (див. Додатковий файл 3) наведені продукти та групи продуктів, що мають відповідні показники сигмоїдоскопії та середні розміри порцій. Загалом 75 продуктів харчування (або груп продуктів) отримали оцінки FSS. Чим вище значення FSS, тим більша асоціація з активністю захворювання і навпаки. Загальна вага продуктів у всіх щоденниках становила 1681 кг. Середній бал сигмоїдоскопії продуктів харчування (тобто показник сигмоїдоскопії продуктів харчування, розрахований для всього набору даних про споживання їжі, становив 2,127). Продукти, виключені з таблиці FSS (таблиця 3), завдяки внеску 2 = 0,07, с
Обговорення
Виразковий коліт вважається генетичним компонентом. Близнюкові дослідження [31] продемонстрували 10% узгодження UC у монозиготних та 3% у двояйцевих близнюків, що свідчить про приблизно 90% екологічного та 10% генетичного внесків. Пул генетично сприйнятливих людей, щонайменше, у 10 разів більший, ніж у тих, у кого діагностовано цей стан. Неможливість визначити відповідальний ген (гени) вказує на складний генетичний компонент із множинними поліморфізмами. Перший гострий епізод UC повинен порушити або екологію, або чутливість та селективність імунної системи до коменсальної кишкової мікрофлори в достатній мірі, щоб викликати хронічний стан. Більш екстремальні версії умов навколишнього середовища, що призводять до подальших рецидивів, могли призвести до першого гострого епізоду.
З усіх дієтичних компонентів, що вивчались стосовно ризику UC та тяжкості захворювання, молоко, мабуть, приділяло найбільшу увагу. Андресон [1] першим висунув постулат, що харчова алергія була причиною UC у двох третин його пацієнтів, і за допомогою елімінаційних дієт стверджували, що ідентифікують порушену їжу та видаляють її. З досвіду Андресона, найпоширенішим провокуючим антигеном було коров’яче молоко. Його погляди підтвердив Роу [32], а пізніше і Truelove [33]. Усі вони постулювали, що чутливість молочного білка є обтяжуючою причиною захворювання приблизно до 5% хворих на колітичну хворобу, яким було вигідно безмолочне харчування. Хоча вони могли продемонструвати циркулюючі антитіла до молочних білків частіше і з вищим титром, ніж у відповідних контролях, вони не змогли співвіднести появу та титр цих антитіл із ступенем, тяжкістю або тривалістю коліту або з реакцією на молоко - безкоштовна дієта. Мішкін [34] дійшов висновку, в огляді теми, що пацієнти з ВЗК уникають молочних продуктів набагато більшою мірою, ніж це може виправдати поширеність мальабсорбції лактози та/або непереносимості молока у цій групі населення. Це спостереження, мабуть, було пов’язано з неправильним сприйняттям пацієнтів та довільними порадами лікарів та авторів популярних книг про дієти.
Для того, щоб з’ясувати, чи можуть дієтичні антигени підтримувати запальну реакцію слизової оболонки, два проспективних контрольованих дослідження досліджували ефективність спокою кишечника та загального парентерального харчування як первинної терапії при лікуванні гострого НК [35, 36]. Жодне з досліджень не виявило жодної переваги порівняно із звичайним лікуванням кортикостероїдами, тому можливість дієтичного антигену, що зумовлює хронічність захворювання, здається малоймовірною. Ці результати узгоджуються з роботою, яка демонструє [37], що роздвоєна ілеостомія не приносить великої користі для лікування UC, але останні спостереження можуть бути збентежені розвитком диверсійного коліту [38].
Незважаючи на те, що індекси клінічної активності використовувались для отримання аналогічних показників балів сигмоїдоскопії продуктів харчування, результати цих вимірювань не включені в цей документ. Індекс клінічної активності передбачає суб’єктивні вимірювання, такі як відчуття благополуччя. Отже, замовлення їжі, отримане за допомогою цих вимірювань, вважалося не таким точним, як замовлення за результатами сигмоїдоскопії.
Консенсус попередніх досліджень щодо дієти та UC вказував на сучасну, оброблену, високо досконалу західну дієту як шкідливу. Представлені тут результати, що пов’язують дієту з діяльністю хвороби, в цілому узгоджуються з цим. Крім того, вони пропонують новий фактор ризику для UC, а саме споживання сульфітованої їжі.
Однак існувала підгрупа (n = 8) цієї популяції, яка реєструвала споживання комплексу вітаміну В або полівітамінів. Ця підгрупа не мала середнього показника сигмоїдоскопії, значно нижчого, ніж загальна популяція UC. Цілком ймовірно, що вітамін В1 є фактором у процесі захворювання, але не єдиним харчовим фактором.
Будь-які дієтичні поради, що надаються хворим на виразковий коліт, повинні ґрунтуватися на таблиці FSS. Таблиця, звичайно, недосконала через помилку експерименту, природні відмінності та асоціації між продуктами харчування. Наприклад, молоко та крупи кодуються окремо, але часто споживаються разом. Таким чином, величина різниці в FSS для цих двох продуктів харчування менша, ніж якби це були незалежні змінні. У ході цього обговорення було зроблено пропозиції щодо факторів, відповідальних за порядок ФСС, та перерахування цих факторів у рекомендації, наведені в таблиці 5 (див. Додатковий файл 5). Ця таблиця є припущенням, оскільки ця дієта не була офіційно перевірена серед населення UC. Однак він представляє єдину вичерпну дієтичну пораду, доступну пацієнтам з виразковим колітом на даний момент.
Список дієтичних факторів ризику раку товстої кишки [42] має схожість з дієтичними факторами ризику, представленими тут для UC. Хворі на UC мають підвищений ризик розвитку раку прямої кишки, і ймовірно, що фактори, відповідальні за запалення у хворих на UC, також відповідають за новоутворення у популяції раку товстої кишки.
Висновок
Описано метод дієтичного аналізу, який пропонує новий інструмент для встановлення взаємозв'язку між дієтою та захворюваннями. Цей метод був застосований для вивчення виразкового коліту і вказує на сульфіт та кофеїн як шкідливі, а тіамін та стійкий крохмаль є потенційно терапевтичними. Вперше розроблено дієтичні рекомендації для хворих на виразковий коліт, включаючи розміри порцій їжі.
- Заспокійливі для живота рецепти хвороби Крона та виразкового коліту
- 20 Виразковий коліт Дієта Поради щодо їжі, яку слід їсти та уникати
- Чи може дієта на основі їжі замінити ексклюзивне ентеральне харчування для пацієнтів з Кроном; s Хвороба AGA
- Аюрведа Виразковий коліт Дієта Поради, домашні засоби
- Асоціація між дієтою та психічним здоров’ям за допомогою 12-позиційної анкети загального стану здоров’я