Озонотерапія послаблює опосередковану NF-кB місцеву запальну реакцію та активацію клітин Th17 при лікуванні псоріазу
Цзіньрон Цзень
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Лі Лей
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Цінхай Цзен
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Юйін Яо
2 Медична школа XiangYa, Центрально-Південний університет, Чанша, Хунань, Китай;
Юцин Ву
2 Медична школа XiangYa, Центрально-Південний університет, Чанша, Хунань, Китай;
Ціньсюань Лі
2 Медична школа XiangYa, Центрально-Південний університет, Чанша, Хунань, Китай;
Ліхуа Гао
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Хунцзяо Ду
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Яцзе Се
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Цзіньхуа Хуан
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Венбін Тан
3 Відділ клітинної біології та анатомії Медичного факультету і
4 Кафедра біомедичної інженерії, Коледж техніки та обчислювальної техніки, Університет Південної Кароліни, Колумбія, Південна Кароліна
Цзянюн Лу
1 Департамент дерматології, Третя лікарня Xiangya, Центральний Південний університет, Чанша, Хунань, Китай;
Пов’язані дані
Анотація
Вступ
Вперше озон був застосований клінічно як стерилізуючий засіб завдяки сильній окислювальній властивості. Він широко застосовується для лікування понад 50 різних патологічних станів, включаючи інфекційні шкірні захворювання 15 - 18, алергічні захворювання 19, 20, лускаті еритеми 21, 22, загоєння ран та відновлення виразки 23. Механізми дії озону можуть лежати в основі антимікробної дії, імунорегуляції, антиоксидантного захисту, епігенетичної модифікації, біосинтезу, анальгетиків та вазодилатації 24. Сучасні озонові медичні препарати для дерматології підпадають під такі основні класифікації: гідротерапія озоном, озонована олія для місцевого застосування, автогемотерапія озоном (OAHT) та порожнина озонового газу/ін’єкція акупунктури 24. Недавні дослідження показали, що точний контроль концентрації озону може спричинити продукцію різних цитокінів, таких як IFN-γ, IL-6 та TNF-α 25. Озон може індукувати та активувати антиоксидантну ферментну систему організму, виробляючи засоби, що поглинають вільні радикали, виводити частину вільних радикалів, що утворюються в результаті запальних реакцій, і перешкоджати виробленню запальних факторів під час розвитку захворювання 26. Однак точні механізми озонотерапії при лікуванні захворювань потребують подальшого з’ясування.
У цьому дослідженні ми оцінили терапевтичну ефективність короткочасного лікування озоном для хворих на псоріаз. Ми досліджували потенційні механізми місцевої озонотерапії псоріазу за допомогою іміквімод- (IMQ) індукованої псоріазоподібної моделі миші. Ми виявили, що озонотерапія послаблює запальні реакції при псоріазі шляхом інгібування шляху NF-κB. Наші результати показують, що озонотерапія є безпечним та ефективним засобом лікування псоріазу і гідна подальших клінічних оцінок та застосувань.
Матеріали та методи
Пацієнти
Це дослідження було схвалено інституційною комісією з огляду (IRB) Третьої лікарні Xiangya, Центральний Південний університет, Чанша, Хунань, Китай. Загалом до дослідження було залучено 10 хворих на псоріаз, у яких діагностовано вульгарний псоріаз, і всі суб’єкти підписали письмові бланки згоди. Клінічна інформація про пацієнтів наведена в Додатковій таблиці 1. Для оцінки активності захворювання використовувались бали PASI. Критерії включення у дослідження були для пацієнтів у віці від 18 до 60 років та із вульгарним псоріазом, діагностованим патологічними дослідженнями. Критеріями виключення були алергія на озоновану воду або масло; вагітність або годування груддю; важкі системні захворювання; і отримавши кортикостероїди, похідні вітаміну D3, інгібітори імунітету, біологічну терапію або пероральні ретиноїди протягом попередніх 2 тижнів.
Мишей BALB/c придбали у Hunan SJA Laboratory Animal Co., Ltd. У віці 6 тижнів самок мишей годували адаптивно протягом 1 тижня та використовували для всіх експериментів. Всіх тварин вирощували та обробляли в експериментальному центрі з тваринами Центрального Південного університету суворо відповідно до відповідних законів та інституційних рекомендацій. Всі процедури на тваринах були схвалені та контролювались Комітетом з догляду та використання медичних тварин Третьої лікарні Сіанья Центрального Південного університету.
Актуальна озонотерапія
Всіх учасників лікували озонованим водяним душем (3,0 ± 1,5 мг/л, HZ-2601B, Hunan Health Care Technology, Чанша, Китай) протягом 15 хвилин, один раз на день, потім обробляли місцевим озонованим маслом (20160522, приблизно пероксидне значення 2000-2,400 ммоль-еквівалент/кг, Hunan Health Care Technology, Чанша, Китай) двічі на день, протягом 14 днів.
Оцінка клінічних фотографій та віддзеркалювальних зображень конфокального мікроскопа на шкірних ураженнях
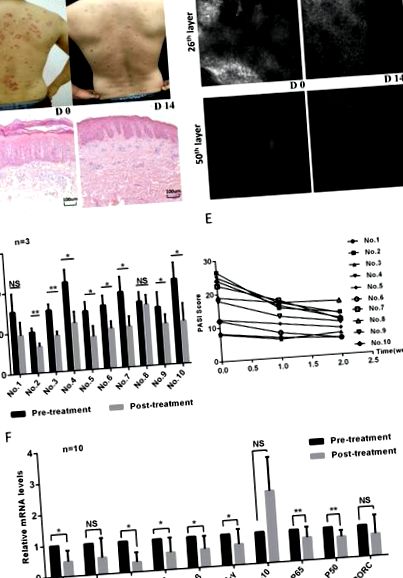
Усі суб'єкти отримували лише безкоштовну озонотерапію; вони не отримували жодних інших методів лікування та ліків під час судового розгляду. Втручання тривало 14 днів. Клінічні фотографії, бали PASI та зображення RCM оцінювали ті самі професійні лікарі, щоб оцінити ступінь тяжкості захворювання до та після лікування. Оцінки PASI включали область уражень шкіри, еритему, масштабування та потовщення, згідно з літературою 27. Кожного суб'єкта оцінювали за допомогою RCM-зображень з трьох різних місць ураження шкіри. Загальна товщина відсканованого RCM шкіри становила 51 шар × 3,05 мкм (вертикально) у кожному шарі. За даними RCM, товщину епідермісу та інфільтровані запальні клітини також оцінювали до та після лікування.
IMQ-індукована мишача модель псоріазу та втручання в озон
Самку мишей BALB/c (у віці 6-8 тижнів) годували у відповідних умовах. Мишей щодня мазали актуальним 5% кремом IMQ (Sichuan Med-Shine Pharmaceutical Co., Ltd., H20030128, Сичуань, Китай) на поголених спинних шкурах протягом 7 днів поспіль. Мишей контрольної групи обробляли такою ж кількістю крему для носія. Усі миші IMQ були випадковим чином розділені на три групи: група, яка не втручалася (група IMQ), група, яка проводила обробку озону (IMQ + озон), і група, що обробляла крем-носій (IMQ + Vehicle). Групу, яка проводила обробку озону, обробляли озонованою водою (HZ-2601B, Hunan Health Care Technology Co., Ltd., Чанша, Китай) протягом 15 хвилин один раз на день, потім обробляли місцевим озонованим маслом (20160522, Hunan Health Care Technology Co ., Ltd., Чанша, Китай). Група для обробки крему для транспортних засобів отримувала водопровідну воду та базове масло з однаковою частотою. Втручання тривало 7 днів. Для оцінки фенотипових характеристик були зібрані клінічні фотографії та оцінки PASI. На 7 день усіх мишей приносили в жертву для збору уражень шкіри, тканин селезінки та лімфатичних вузлів.
Виділення CD4 + Т-клітин
Одноядерні клітини периферичної крові (РВМС) відокремлювали від периферичної крові пацієнтів до і після лікування центрифугуванням із використанням середовища з градієнтом щільності (GE Healthcare, Чикаго, Іллінойс, США). CD4 + Т-клітини виділяли шляхом позитивного відбору з використанням кульки Miltenyi відповідно до інструкцій виробника (Miltenyi Biotec, Bergisch Gladbach, Німеччина). Далі, виділені CD4 + Т-клітини збирали для подальших експериментів. В експерименті з мишами CD4 + Т-клітини очищали від об'єднаних одноклітинних суспензій селезінки, використовуючи комплект для ізоляції CD4 + Т-клітин миші від Miltenyi Biotec (Бергіш Гладбах, Німеччина).
Проточна цитометрія
Загальну РНК екстрагували з клітин або тканин шкіри за допомогою TRIzol відповідно до інструкцій виробника (Thermo Fisher Scientific, Waltham, MA, USA). ІРНК транскрибували за допомогою набору реактивів PrimeScript ® RT (Takara Biomedical Technology Co., Ltd., Кусацу, Шига, Японія) з 1 мкг загальної РНК у кожній реакції. Реакційна суміш для ПЛР у режимі реального часу містила 2 мкл кДНК, 10 мкл SYBR Premix Ex Taq ™ (Takara Biomedical Technology Co., Ltd., Кусацу, Шига, Японія) і 400 нМ чутливих та антисмислових праймерів для остаточного об'єм 20 мкл. QPCR проводили на термоциклері LightCycler ® 96 (Roche, Rotkreuz, Швейцарія). Кількість експресії гена розраховували за допомогою методів 2 -ΔCt і нормалізували до гліцеральдегід-3-фосфатдегідрогенази (GAPDH). Грунтовки наведені в додатковій таблиці 2.
Вестерн-блотинг
CD4 + Т-клітини лізували, а білки екстрагували за допомогою реактора для ядерної екстракції (Boster Biological Technology, Pleasanton, CA, USA). Кількісно визначали білки за допомогою реагенту Бредфорда (Thermo Fisher Scientific, Waltham, MA, USA), після чого проводили 12% вертикальний електрофорез додецилсульфату та поліакриламідного гелю. Потім білки переносили в мембрану полівінілідендіфториду (PVDF) (Sigma-Aldrich, Сент-Луїс, Міссурі, США). Мембрану PVDF блокували в 5% знежиреному молоці протягом 1 години при кімнатній температурі, потім інкубували з антитілом проти P65 (GB11142, 1: 1000, Wuhan Servicebio Technology Co., Ltd., Ухань, Китай) або P50 (ab7971, 1: 5000, Abcam, Кембридж, Массачусетс, США) протягом 12-16 год при 4 ℃, з подальшою інкубацією з антитілами IgG проти кролика миші (H&L) (GenScript, Piscataway, NJ, USA). Білки виявляли за допомогою посиленого хемілюмінесцентного (ECL) вестерн-блот-детектуючого набору (Thermo Fisher Scientific, Waltham, MA, USA). Кількісне визначення P65 та P50 нормалізували до GAPDH методом денситометрії.
Гістологічний аналіз
Тканини шкіри всіх пацієнтів та мишей фіксували у формаліні та вбудовували у парафін (Wuhan Servicebio Technology Co., Ltd., Wuhan, China). Зрізи (6 мкм) фарбували гематоксиліном та еозином і зберігали при кімнатній температурі. Оцінювали товщину епідермісу та інфільтруючі запальні клітини.
Імуногістохімічне фарбування
Зрізи (6 мкм) фарбували антитілами P50 (№ за каталогом BS1249, Bioworld Technology Co., Ltd., Нанкін, Китай), P65 (№ за каталогом 10745-1-AP, Proteintech, Rosemont, IL, США) та TLR2 антитілами (№ за каталогом ab213676, Abcam, Кембридж, Массачусетс, США) відповідно до інструкцій виробника. Аналіз зображення проводили за допомогою флуоресцентного мікроскопа та програмного забезпечення для аналізу Leica Qwin Std (Leica, Wetzlar, Німеччина).
Високопропускна послідовність
Отримані транскриптомні профілі лівої та правої сторін уражень шкіри від моделей самоконтролю мишей та уражень спинних шкір миші в контрольній групі та групі IMQ. Коротко, із цих зразків шкіри було виділено загальну РНК; мРНК збагачували, фрагментували і використовували для синтезу кДНК. Фрагменти кДНК ампліфікували за допомогою ПЛР, а розмір і якість бібліотеки секвенування визначали за допомогою біоаналізатора Agilent 2100 (Agilent, Санта-Клара, Каліфорнія, США). Бібліотеку секвенували за допомогою високопродуктивної платформи секвенування HiSeq X Ten (Illumina Inc., Сан-Дієго, Каліфорнія, США). Диференціально експресовані гени серед вибраних зразків були проаналізовані за допомогою Кіото-енциклопедії генів і геномів (KEGG).
Статистичний аналіз
Місцеве лікування озоном значно пригнічує передачу сигналів TLR2/NF-κB. (а) Рівні експресії TLR2, P50 та P65 при ураженнях шкіри з груп Ctrl, IMQ, IMQ + Vehicle та IMQ + Озон оцінювали за допомогою імуногістохімічного аналізу. (b) Рівні експресії TLR2, P50 та P65 при IMQ-індукованих самоконтрольних ураженнях шкіри миші та (c) ураження псоріазу людини до та після лікування озоном.
Придушення диференціації Th17 шляхом місцевого лікування озоном
Псоріаз - це хронічне рецидивуюче запальне захворювання шкіри. Ми стверджуємо, що озонотерапія може контролювати прогресування псоріазу, пригнічуючи запальну реакцію уражень шкіри. Дослідження виявили, що озонована олія не тільки забезпечує реактивний кисень, але й підтримує терапевтично активні похідні озонованих речовин протягом тривалого часу 38. Наші попередні дослідження показали, що озоноване масло є безпечним та ефективним для лікування стійкого вульгарного псоріазу з ефективністю, еквівалентною глюкокортикоїдів проміжної дії 39. У цьому дослідженні ми продемонстрували, що псоріатичні ураження шкіри пацієнтів значно пом'якшуються і що запальні біомаркери, такі як IL-17a, IL-6, TNF-α, TGF-β та IFN-γ, суттєво знижуються після обробки озоном. Ми також показали, що озонотерапія може суттєво інгібувати пов'язані із запаленням шляхи, такі як NF-κB, TLR, TNF та IL-17, на тваринній моделі псоріазу. Ці дані дають уявлення про механізми терапевтичного впливу озонотерапії на псоріатичні ураження.
Активація клітин Th17 має вирішальне значення для запальної реакції на ураження псоріазу vulgaris 51. Наші результати показують, що лікування озоном може суттєво пригнічувати індуковане IMQ збільшення кількості та активної функції клітин Th17. Активація сигнального шляху NF-κB може індукувати активацію клітин Th17 52. Отже, опосередковане озоном придушення активації клітин Th17, ймовірно, зумовлене інгібуванням шляхів NF-κB. На додаток до клітин Th17, інші запальні клітини, такі як Th1, Th2, дендритні клітини (DC), клітини природних кілерів (NK) та макрофаги, також беруть участь у запальній реакції псоріазу 53. Однак наші результати показують, що лікування озоном має мінімальний вплив на ці клітини. Отже, озон, ймовірно, має специфічний вплив на регуляцію клітин Th17 під час лікування псоріазу.
На додаток до озонованої води та нафти, також повідомляється, що озоновая автогемотерапія та порожнина озонового шару/ін’єкція акупунктури покращують антиоксидантну здатність організму та регулюють запалення 54 - 56. Чи можна застосовувати ці методи лікування псоріазу, ще не встановлено. Озон також можна використовувати в поєднанні з іншими препаратами з метою зменшення побічних ефектів та підвищення ефективності. Наприклад, комбінована інтрадискальна та периангліонарна ін’єкція медичного озону та стероїдів має кумулятивний ефект, що призводить до загальних результатів лікування болю, спричиненого грижею диска 57. Місцева озонотерапія має кілька побічних ефектів, таких як подразнюючий біль. Це рідко викликає системні побічні ефекти. У цьому дослідженні є деякі обмеження. Наприклад, відсутні дані щодо довгострокової ефективності лікування або його впливу на частоту рецидивів. На питання про те, чи відіграє озон регулюючу роль у розповсюдженні та диференціації кератиноцитів та у вазодилатації псоріазу, досі не отримано відповіді.
- Озонотерапія Меридіан Натуропатичний лікар Бойсе Центр Карлфельдта
- Переваги та побічні ефекти від озонотерапії - TipsHire Найкращі огляди продуктів за один клік
- Клітини-попередники строми з ендогенної жирової тканини сприяють перицитам і адипоцитам, які
- Приємна та ефективна водна терапія для схуднення - Кращі рецепти - Сабі Гіст
- Лікування ожиріння - роль для ерготерапевтів Скандинавський журнал трудової терапії