Ожиріння, пов’язане з пролактиномою, що лікується бупропіоном та метилфенідатом
Ян Терок
Кафедра психіатрії та психотерапії, Любецький університет, Ratzeburger Allee 160, Любек, 23538, Німеччина
Фріц Хогаген
Кафедра психіатрії, Любецький університет, Любек, Німеччина
Дірк Петерсен
Інститут нейрорадіології, Університет Любека, Любек, Німеччина
Бартош Зуровський
Кафедра психіатрії, Любецький університет, Любек, Німеччина
Вступ
Ожиріння було сильно пов'язане з дофамінергічною недостатністю та дисфункціональною процедурою винагороди [Wang et al. 2001; Джонсон і Кенні, 2010]. Дофамін пропонується регулювати споживання їжі, модулюючи пов'язані з їжею сигнали винагороди в межах мезолімбічної циркуляції мозку [Martel and Fantino, 1996], а також регулюючи периферичну функцію адипоцитів [Ben-Jonathan and Hnasko, 2001]. Збільшення споживання їжі трактується з точки зору компенсації основного дофамінергічного дефіциту, включаючи зниження фазових сигналів винагороди до харчових стимулів. Послідовно пацієнти, які отримують сполуки, що блокують D2-рецептори, відзначають підвищений апетит та збільшення ваги [Baptista, 1999]. І навпаки, ліки, що підвищують рівень дофаміну в мозку, сприяють зменшенню ваги та апетиту. [Towell et al. 1988; Фолтін та ін. 1990]. Аденоми гіпофіза, що секретують пролактин, можуть служити механічно вірогідним прикладом для дослідження ролі дофаміну в ожирінні. Пролактиноми пригнічують дофамінергічний тонус і, як показано, послідовно пов’язані із збільшенням маси тіла та ожирінням [Greenman et al. 1998]. Показано, що подібні ураження головного мозку, що призводять до ожиріння, пов’язані зі зниженим дофамінергічним тонусом, наприклад гіпоталамічні пухлини, такі як краніофарингіома [Elfers and Roth, 2011].
Тим не менш, точний механізм асоціації пролактиноми та ожиріння недостатньо вивчений, і дослідження ожиріння після нормалізації рівня пролактину показують суперечливі результати [Greenman et al. 1998; Delgrange та ін. 1999; дос Сантос Сільва та ін. 2011]. Однак як стандартне фармакологічне лікування пролактиноми, так і когнітивно-поведінкове лікування часто не дозволяють зменшити вагу пацієнтів [Doknic et al. 2002; дос Сантос Сільва та ін. 2011]. Загалом існує значна потреба у ефективних клінічних варіантах боротьби з ожирінням, пов'язаних з пухлинами гіпофіза, та для з'ясування взаємозв'язку центрального та периферичного ефектів дофаміну на адипогенез, включаючи роль пролактину. Вищезазначені спостереження пропонують дослідити нові дофамінергічні стратегії.
Опис справи
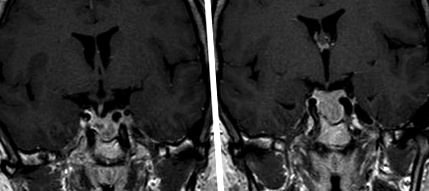
Ми прийняли 35-річного пацієнта (НР) до нашого стаціонарного психіатричного відділення через 1 рік після діагностики аденоми, що секретує пролактин (макропролактинома, див. Рисунок 1).
Зріз T1-зваженого МРТ, що показує макропролактиному NR розміром 26 мм × 20 мм × 19 мм (ліворуч-право; черепно-каудальний; передній-задній). Подальше обстеження виявило, що гіпофіз та стебло гіпофіза зміщені праворуч. Проліферація тканини сіркової тканини поширюється на супраселярну та ліву параселярну області без стиснення хіазми зорового нерва. Ліва внутрішня сонна артерія була огороджена оточуючими м’якими тканинами. Праворуч пухлина поширювалася на краніомедіальну частину сонної артерії.
Проведення МРТ показало постійне зменшення обсягу гіпофіза. Отже, пацієнт пройшов дві тривалі стаціонарні процедури, спрямовані на зменшення ваги в різних лікарнях із застосованим когнітивно-поведінковим підходом. Обидва способи лікування були неефективними, без зменшення ваги після першого лікування і навіть збільшення ваги після другого лікування.
При надходженні маса тіла NR становила 142,7 кг, з індексом маси тіла (ІМТ) 50,6. Під впливом їжі він виявлявся імпульсивним та знеціненим, їв більшу кількість, не враховуючи наслідків. Однак ці події не відповідали критеріям запоїв.
Загалом, NR демонстрував дефіцит стійкої уваги та терпіння, коли стикався з неприємними повсякденними завданнями. Симптомами афективної лабільності були регулярні, але короткі епізоди смутку, гніву чи щастя. Більше того, він виявив нереальні та регулярно мінливі плани на майбутнє, наприклад, ставши професійним тенісистом. NR повідомляє, що страждає від наслідків надмірної ваги, що ускладнює пошук друзів або партнера. Структуроване клінічне інтерв'ю згідно DSM-IV не виявило доказів первинного психічного розладу, зокрема розладу настрою, розладу харчування або розладу уваги з гіперактивністю (СДУГ). Це було підтверджено застосуванням специфічних шкал оцінок для конкретних захворювань. Ми розпочали лікування, зосередившись на афективних симптомах, з 300 мг бупропіону, норадреналіну та інгібітора зворотного захоплення дофаміну. Через 3 тижні афективні симптоми покращились; все ж залишалася імпульсивна та необдумана поведінка. Більше того, пацієнт втратив 1,5 кг ваги.
На 6-му тижні ми додали метилфенідат, починаючи з 18 мг і збільшуючи дозу до 36 мг на 7-му тижні. Комбінований препарат добре переносився, NR повідомляв, що він має довшу та кращу здатність зосереджувати свою увагу або організовувати завдання. Ми спостерігали менш імпульсивну та цілеспрямовану поведінку з покращеною емоційною стабільністю. Крім того, неконтрольоване споживання їжі та вага тіла зменшились без будь-яких повідомлень або спостережуваних зусиль, щоб взяти під контроль імпульс до їжі. Ми виписали NR з масою тіла 133 кг (ІМТ 47,1) після 10 тижнів лікування. Жодного разу ми не застосовували психологічне лікування ожиріння і не ставили вагу тіла головною проблемою в терапевтичних сеансах та відвідуваннях. НР явно відмовлявся від будь-яких зусиль щодо схуднення.
Ми бачили пацієнта для подальших співбесід через 3 та 8 тижні після виписки. Психопатологічний статус Н.Р. та його вага залишались по суті стабільними, з невеликим зростанням до 134,1 кг (+1,1). Ліки залишалися незмінними і добре переносились. Через вісім тижнів після виписки вага тіла NR ще більше зменшилась до 131,8 кг.
Обговорення
Ми представляємо, наскільки нам відомо авторам, перший звіт про комбіноване лікування бупропіоном та метилфенідатом, додане до встановленої терапії каберголіном у пацієнта з аденомою гіпофіза, що секретує пролактин. Ми повідомляємо про подальше поліпшення нервово-психічних симптомів та стійке зменшення ожиріння. Цього поліпшення не спостерігалось під час попереднього 1-річного лікування каберголіном, незважаючи на нормалізацію рівня пролактину, соматотропіну та тестостерону. Це спостереження свідчить про відсутність прямого впливу цього агоніста D2 на систему обробки винагороди та непрямого впливу на вагу через нормалізацію рівня пролактину.
Примітно, що порушення циркадного ритму секреції пролактину, а не базового рівня пролактину, були пов’язані із збільшенням ваги [Doknic et al. 2002], що може пояснити деякі невідповідності у згаданій вище літературі [Greenman et al. 1998; Delgrange та ін. 1999; дос Сантос Сільва та ін. 2011]. Оскільки рівень соматотропіну нормалізувався на момент лікування, ми не замінювали цей гормон. Нормалізація рівня соматотропіну без будь-якого впливу на масу тіла припустила, що заміна соматотропіну не призвела б до значного впливу на масу тіла. Крім того, гіпосоматотропінемія швидше асоціюється із селективно підвищеним вісцеральним жиром, ніж із ожирінням. Тим не менш, суттєвий ефект заміни очевидно можливий.
Однак слід враховувати інші причини зменшення ваги. Слід враховувати наслідки самого госпіталізації. Однак як відсутність зменшення ваги протягом двох попередніх терапій, спрямованих на зменшення ваги, так і підтримка зниження ваги через 8 тижнів після виписки, роблять в основному екологічне пояснення малоймовірним. Нарешті, ми не можемо розрізнити прямий фармакологічний вплив на регулювання їжі та побічно знижене споживання їжі через клінічне поліпшення, пов’язане з поліпшенням контролю та гальмування поведінки.
Незважаючи на те, що інші внески не можна виключати, немає жодних натяків на інші причинні фактори ожиріння пацієнта. Раніше він пройшов детальний діагностичний процес, що включав широкий діапазон лабораторних показників (включаючи тест на GnRH та індукований інсуліном тест на гіпоглікемію), повторне сканування мозку МРТ, генетичний аналіз на рівні генів та хромосом, не виявляючи ніяких відхилень від норми. вже згадані. Більше того, біографія пацієнта не має травмуючих подій або навіть серйозних викликів у контексті дуже доброго батьківського піклування, не має сімейної історії надмірної ваги або ожиріння. У сукупності пролактиному пацієнта можна розглядати як достатню для виникнення спостерігається дефіциту, і в даному випадку пропонує найбільш вірогідне пояснення.
Питання про відносний внесок бупропіону та метилфенідату, включаючи їх можливу синергію, не може бути вирішене у цій справі. Незначна втрата ваги, яка спостерігається вже лише при застосуванні бупропіону, свідчить про те, що цей препарат сприяв ефекту, який спостерігався після додавання метилфенідату. Тим не менше, спостерігається стійке зниження ваги робить комбінацію бупропіону та метилфенідату перспективною стратегією, що заслуговує на подальше дослідження. Це стосується, принаймні, терапії рефрактерного ожиріння, пов’язаного з пухлинами головного мозку гіпофіза, які можуть недостатньо лікуватися каберголіном або бромокриптином щодо вагових аспектів. Більше того, поєднання цих трьох дофамінергічних препаратів (каберголін, бупропіон та метилфенідат) добре переносилось і не призвело до якихось специфічних побічних ефектів, що на сьогоднішній день не описано в літературі. Однак з цього звіту про випадки не можна отримати певної інформації про безпеку. Слід враховувати особливо вплив на зниження судомного порогу у пацієнтів з епілепсією, але також вплив на інші супутні захворювання. Загалом, наші результати підтверджують роль дофамінергічної недостатності та дисфункціональної обробки винагород у цьому, ще недостатньо зрозумілому стані [Greenman et al. 1998].
Виноски
Фінансування: Це дослідження не отримало жодного конкретного гранту від жодної фінансової установи у державному, комерційному або некомерційному секторах.
Інформація про учасника
Ян Терок, кафедра психіатрії та психотерапії, Любецький університет, Ratzeburger Allee 160, Любек, 23538, Німеччина.
Фріц Хогаген, кафедра психіатрії, Університет Любека, Любек, Німеччина.
Дірк Петерсен, Інститут нейрорадіології, Університет Любека, Любек, Німеччина.
Бартош Зуровський, кафедра психіатрії, Університет Любека, Любек, Німеччина.
- Запобігання ожирінню у мишей, які отримували наночастинки, що відключають ген, Technology Org
- Не придатний до боротьби Як ожиріння загрожує американським військовим
- Метаболічний; Ожиріння; Відділ ендокринології; Медичний коледж; Університет Флориди
- Метаболічно здорове ожиріння та ризик зниження функції нирок - Чанг - 2018 - Ожиріння - Уайлі
- Прогресивний характер ожиріння та діабету у нелюдських приматів - Хансен - 2017 - Ожиріння - Вілі