Нова стратегія використання лептину для терапії ожиріння
Анотація
Вступ
Ожиріння є хронічним захворюванням і головним глобальним викликом здоров’ю. Окрім баріатричної хірургії, яка коштує дорого і не позбавлена ризику, в даний час не існує успішних варіантів довгострокового лікування ожиріння. Історія фармакологічних засобів для ожиріння була бурхливою, і багато прикладів виведення препаратів з ринку через значні побічні ефекти. Орлістат та сибутрамін (найновіші препарати на ринку) забезпечують лише помірне зниження ваги, і обидва вони пов’язані з високими показниками зносу через нестерпні побічні ефекти. Крім того, нещодавно сибутрамін був вилучений з ринку. Існує потреба у розробці безпечних та ефективних медикаментозних методів лікування ожиріння.
Території покриті
Історія терапії лептином як препаратом-сиротою, замісної лептину як лікування ожиріння, доклінічні дослідження, що показують ефективність комбінації лептину/аміліну і, нарешті, дуже перспективні ранні клінічні висновки з використанням комбінованої терапії прамлінтидом/метелептином у осіб із надмірною вагою та ожирінням.
Висновок експерта
Комбінована фармакологічна терапія, така як прамлінтид/метрелептин, для лікування ожиріння є дуже перспективною і підтримується заохоченням результатів зниження ваги та покращенням обміну речовин у клінічних дослідженнях на ранніх стадіях. Однак останнє рандомізоване клінічне випробування прамлінтиду/метрелептину нещодавно було припинено через проблеми безпеки.
1. Вступ
При фармакологічній розробці нових препаратів для лікування ожиріння безпека препарату є першорядною і повинна розглядатися шляхом зважування ризиків для людини від ожиріння та можливих проблем, які можуть виникнути при лікуванні наркотиками. На жаль, історія фармакологічного лікування ожиріння була бурхливою здебільшого через проблеми безпеки [1,2]. Ожиріння - це хронічне захворювання, яке має безліч причин, і все це призводить до стійкого дисбалансу між споживанням енергії та витратами енергії. Виниклий в результаті надлишок жирової тканини пов’язаний з більш високим ризиком розвитку багатьох захворювань, включаючи діабет 2 типу та серцево-судинні захворювання, деякі типи раку, інвалідність, ускладнення легеневого та шлунково-кишкового тракту, а також депресію [3]. Як і очікувалося від такої складної хвороби, що виникає в результаті взаємодії між навколишнім середовищем та безліччю генів сприйнятливості, лікування є рідкісним, і лікування таким чином спрямоване на паліацію. Яким би не було основне місце дії фармакологічного агента, чистий ефект повинен бути зменшенням споживання їжі та/або збільшенням витрат енергії.
Поодинокі агенти загалом дуже обманювали, і зараз лікарі майже не мають довгострокових фармакологічних засобів для лікування захворювання. Однак після популярного успіху Fen-Phen, поєднання фенфлураміну та фентерміну, у 1980-х [4] стало зрозуміло, що для успішного лікування ожиріння необхідна комбінація препаратів, незважаючи на те, що фенфлурамін був виведений з ринку в 1996 р. Через смертельну легеневу гіпертензію. Враховуючи поганий довгостроковий успіх з дієтичними втручаннями та помірну ефективність та тривалі проблеми безпеки, пов’язані з аноректичними малими молекулами, існує нагальна потреба у нових підходах, які перетворюють наукові досягнення на інноваційні методи лікування, які пропонують тривале, клінічно значуще зниження ваги з мінімальними побічні ефекти. Такі цілі змусили багато фармацевтичних та біотехнологічних компаній розпочати рандомізовані подвійні сліпі клінічні випробування з використанням комбінацій існуючих препаратів для лікування ожиріння. Нещодавно було запропоновано потенційне використання раціонального та перспективного комбінаторного нейрогормонального підходу з використанням пептидних гормонів, які відіграють фізіологічну роль у регулюванні споживання їжі та маси тіла та потенційно позбавлені нецелевих токсичних речовин.
Графа 1. Резюме лікарських засобів
| Назва препарату | Прамлінтид ацетат | Метрелептин (рекомбінант-метіоніловий лептин людини) |
| Фаза | FDA затверджено, березень 2005 р | На фазі III |
| Індикація | Діабет 1 типу: підтримуюча доза 30 або 60 (у міру переносимості), титрована з дози 15 мг Інсулін, що застосовує діабет 2 типу: підтримуюча доза 120 мкг (у міру переносимості), титрувана з дози 60 | Вроджена недостатність лептину, ліподистрофія, гіпоталамічна аменорея та замісна терапія лептином для підтримки ваги |
| Опис фармакології | У клінічних дослідженнях у пацієнтів з діабетом 2 та 1 типу, які застосовують інсулін, введення прамлінтіду призвело до зменшення середніх концентрацій глюкози після їжі, зменшення коливань глюкози та зменшення споживання їжі Пік: 15 хв [50] Період напіввиведення: 20 - 50 хв [50,51] | За результатами неклінічних та клінічних досліджень механізми дії метрелептину включають наступне: • Корекція гіперфагії, вторинної внаслідок дефіциту лептину, та супутнє зменшення споживання калорій та жиру [52,53] • Стимуляція окислення жирних кислот у всьому тілі та зниження рівня ліпідів у плазмі, печінці та міоцелюлярних ліпідах, що призводить до підвищення чутливості до інсуліну та поліпшення глікемічного контролю [54-61] • Поліпшення придушення інсуліну вироблення глюкози в печінці та збільшення стимульованого інсуліном периферичного засвоєння глюкози в м’язах [20,54,62] Отже, лептин діє за допомогою різноманітних механізмів для зменшення тригліцеридів та інших проміжних продуктів ліпідів у пацієнтів з ліподистрофією, зменшуючи їх накопичення в тканинах, таких як печінка та м’язи, та покращуючи важку резистентність до інсуліну, тим самим покращуючи гіперглікемію та гіпертригліцеридемію Пік: 4 год [63] Період напіввиведення: 2 - 5 годин [63,64] |
| Шлях введення | Вводять підшкірно в стегно або живіт, окремо від місця ін’єкції інсуліну безпосередньо перед основними прийомами їжі (≥ 250 ккал або ≥ 30 г вуглеводів) | Вводять підшкірно в живіт |
| Хімічна структура | Lys-Cys-Asn-Thr-Ala-Thr-Cys-Ala-Thr-Gln- Arg-Leu-Ala-Asn-Phe-Leu-Val-His-Ser-Ser- Asn-Asn-Phe-Gly-Pro-Ile-Leu-Pro-Pro-Thr- Asn-Val-Gly-Ser-Asn-Thr-Tyr-NH2 ацетат (сіль) з дисульфідним мостом між двома залишками Cys [65] | NH2-Met-Val-Pro-Ile-Gln-Lys-Val-Gln-Asp-Asp-Thr-Lys- Thr-Leu-Ile-Lys-Thr-Ile-Val-Thr-Arg-Ile-Asn-Asp-Ile-Ser- His-Thr-Gln-Ser-Val-Ser-Ser-Lys-Gln-Lys-Val-Thr-Gly-Leu- Asp-Phe-Ile-Pro-Gly-Leu-His-Pro-Ile-Leu-Thr-Leu-Ser-Lys- Met-Asp-Gln-Thr-Leu-Ala-Val-Tyr-Gln-Gln-Ile-Leu-Thr- Ser-Met-Pro-Ser-Arg-Asn-Val-Ile-Gln-Ile-Ser-Asn-Asp- Leu-Glu-Asn-Leu-Arg-Asp-Leu-Leu-His-Val-Leu-Ala-Phe- Ser-Lys-Ser-Cys-His-Leu-Pro-Trp-Ala-Ser-Gly-Leu-Glu- Thr-Leu-Asp-Ser-Leu-Gly-Gly-Val-Leu-Glu-Ala-Ser-Gly- Tyr-Ser-Thr-Glu-Val-Val-Ala-Leu-Ser-Arg-Leu-Gln-Gly- Ser-Leu-Gln-Asp-Met-Leu-Trp-Gln-Leu-Asp-Leu-Ser-Pro- Gly-Cys-COOH |
| Ключове випробування | Діабет 1 типу: [66-68] Діабет 2 типу: [69-71] | Вроджений дефіцит лептину [18] Ліподистрофія: [20] Гіпоталамічна аменорея: [22] Ожиріння: [26,48] Підтримка ваги: [38] |
2. Короткий зміст прамлінтіду та метрелептину
Прамлінтид ацетат, синтетичний аналог аміліну, вводять шляхом підшкірної ін’єкції перед основними прийомами їжі, щоб знизити екскурсії після їжі глюкози у діабетиків 1 та 2 типів. Амілін - це 37-амінокислотний пептидний гормон, який секретується з інсуліном β-клітинами підшлункової залози. Подібно до інсуліну, концентрація аміліну в плазмі швидко зростає у відповідь на прийом їжі, досягаючи максимуму приблизно через 30 хв після їжі та повертаючись до вихідного рівня приблизно через 2 год [11]. Повідомлялося про рівень аміліну натще у здорових людей у межах 3 - 25 пмоль/л [12]. Реакція аміліну на прийом їжі відсутня при цукровому діабеті 1 типу (T1DM), перебільшена при ожирінні і зменшена при цукровому діабеті 2 типу (T2DM).
Людський амілін, як правило, нерозчинний і має тенденцію до агрегації, що виключає терапевтичне використання його природного пептиду. Для боротьби з цим розчинний неагрегуючий рівносильний аналог аміліну людини прамлінтид був розроблений та затверджений FDA у 2005 р. Прамлінтид представлений як ацетатна сіль синтетичного 37-амінокислотного поліпептиду, що відрізняється амінокислотною послідовністю з аміліну людини шляхом заміни на пролін у положеннях 25 (аланін), 28 (серин) і 29 (серин) і має молекулярну масу 3949,4 Да. Фармокінетичні дослідження показали, що дози прамлінтіду 30 і 60 мкг у пацієнтів з діабетом 1 типу та 120 мкг у хворих на цукровий діабет 2 типу дають концентрацію прамлінтиду в плазмі, яка наближається до фізіологічних концентрацій аміліну у здорових суб'єктів. Найпоширеніші побічні ефекти у споживачів прамлінтіду пов'язані з шлунково-кишковими подіями, включаючи блювоту, нудоту та біль у животі. Крім того, прамлінтид як допоміжне лікування у пацієнтів, які використовують інсулінотерапію під час прийому їжі, та одночасне застосування прамлінтіду з інсуліном можуть збільшити ризик інсулінової гіпоглікемії, особливо у пацієнтів з діабетом 1 типу [13]. Фармокінетика та фармодинаміка прамлінтіду були добре описані в опублікованих раніше оглядах [14,15].
Метрелептин, також відомий як рекомбінантний метіоніл людський лептин, є аналогом людського гормону лептину. Для експресії метрелептину в кишковій паличці послідовність, що кодує зрілий білок людського лептину (146 амінокислот), була хімічно синтезована з використанням оптимальних кодонів E. Як частина цього синтезу, нуклеотиди ATG (що кодують метіонін) були додані до 5 ’кінця гена людського лептину. Отже, протеїн метрелептину, кодований цією послідовністю, має довжину 147 амінокислот, починаючи з метіоніну, і має розрахункову молекулярну масу 16 156 Да. Лікування метрелептином в основному проводилося пацієнтам із вродженою недостатністю лептину, ліподистрофією та гіпоталамічною аменореєю.
3. Лептин як сирота-препарат у людей
Перші докази, які вказували на можливе використання замісної лептинової терапії при ожирінні, з’явилися в 1997 р., Коли О’Рахіллі та його колеги виявили двох дітей із сильним ожирінням, які мали мутацію гена лептину [16]. Ці двоє дітей були двоюрідними братами родини пакістанського походження з дуже спорідненою родиною, у яких обох була гомозиготна мутація із зміщенням кадрів, що включала делецію одного нуклеотиду гуаніну в кодоні 133 гена лептину. Це призвело до дуже низького рівня лептину в циркуляції, екстремальної гіперфагії та важкого ожиріння [16]. Ці дослідники далі показали, що щоденні підшкірні ін'єкції рекомбінантного людського лептину протягом 4 років можуть покращити гіперфагію, надмірне збільшення ваги в ранньому віці та важке ожиріння у цих дітей [17]. У дослідженні конкретного випадку щоденні підшкірні ін’єкції рекомбінантного лептину (0,028 мг/кг) вводили протягом 12 місяців у 9-річної дівчинки з вродженим дефіцитом лептину. На початковому рівні пацієнт важив 94,4 кг (> 99,9-й процентиль за віком), зріст становив 91-й процентиль (з урахуванням віку кісток), а рівень лептину в сироватці крові був нижчим за межу виявлення. Після лікування лептином пацієнт втратив 16,4 кг (
Замісна терапія лептином також виявилася безпечною та ефективною терапією для лікування гіпоталамічної аменореї (ГА), розладу, що характеризується припиненням менструальних циклів, як правило, спричиненим хронічним дефіцитом енергії, що виникає внаслідок сильних фізичних навантажень та/або зменшення споживання їжі, наприклад у хворих на нервову анорексію [22,23]. Жінки з ГК, як правило, гіполептинемічні [24,25]. Дослідження, що підтверджує концепцію, показує, що 3 місяці замісної терапії лептином не лише нормалізували рівень естрогену, гормонів щитовидної залози та IGF-1, але найголовніше - відновлювали овуляторні менструації [22 ]. Подальше рандомізоване подвійне сліпе плацебо-контрольоване дослідження, що тривало 36 тижнів замісної терапії людським рекомбінантним лептином (метрелептином) у жінок з ГК, виявило подібні покращення стану гонад, щитовидної залози, гормону росту та очей надниркових залоз, але також продемонструвало поліпшення маркерів кісткового метаболізму, що свідчить про формування кісток [23].
4. Застосування лептину в клінічних випробуваннях із ожирінням
Навпаки, обіцянка лептину як самостійної магічної кулі для лікування ожиріння була недовгою. У 1999 р. Було проведено рандомізоване контрольоване дослідження реакції на дозу щоденного введення підшкірного рекомбінантного лептину у 54 худих та 73 осіб із ожирінням. На початковій фазі дослідження, яке тривало 4 тижні, худі та ожирілі пацієнти втрачали однакову кількість ваги при лікуванні лептином, що було статистично значущим порівняно з вихідним рівнем (р = 0,02) [26]. Суб'єкти з ожирінням вивчалися ще 20 тижнів. З 47 пацієнтів, які закінчили дослідження, 8, які отримували найвищу дозу лептину, втратили 7,1 кг (р = 0,01 порівняно з вихідним рівнем), тоді як ті, хто отримував плацебо, втратили 1,3 кг. Ефекти сильно варіювали серед пацієнтів, від втрати близько 15 кг до приросту 5 кг у групі, яка отримувала найвищу дозу. Крім того, ці дози викликали подразнення шкіри та набряк у місці ін'єкції у 62% пацієнтів та головний біль у половини пацієнтів. Надія на те, що лептинова терапія буде ліками від ожиріння, зникла після цього випробування, незважаючи на численні спроби Amgen Pharmaceuticals продовжити подальші дослідження гормону, який, на думку багатьох дослідників, був би панацеєю для лікування ожиріння.
5. Стратегія заміщення лептину при терапії ожиріння
Підтримання зниженої маси тіла супроводжується метаболічною реакцією, яка спрямована на захист від подальшої втрати ваги. Ця реакція характеризується падінням енергетичних витрат за межі передбаченого змінами в складі тіла [27-29], притупленням нейроендокринних функцій (пригнічуються щитовидна та репродуктивна осі, знижується симпатична активність і посилюється парасимпатична активність) та рівень циркулюючого лептину збільшуються. Ця метаболічна адаптація до обмеження калорій пояснює, принаймні частково, відновлення втраченої маси тіла з часом і, схоже, пов’язана із падінням лептину, яке відбувається при втраті ваги [30-32]. Було запропоновано, що основна фізіологічна роль лептину - не як сигнал ситості - захищати запаси жиру в організмі в умовах тривалого дефіциту енергії [33-35].
Екзогенне лептин-індуковане відновлення репродуктивної, щитоподібної та надниркової осей разом із збільшенням маркерів формування кісток у жінок із вторинною аменореєю та гіполептинемією (тобто індукованою хронічним дефіцитом енергії) підтримало б гіпотезу відновлення центральної чутливості до лептину [22, 23]. Погоджуючись з цим, метрелептин лише змінив метаболічний фенотип осіб з обмеженим вмістом калорій, коли циркуляція лептину значно зменшилась на 30% і зберігалася протягом декількох тижнів [38,39], а не у осіб, у яких циркулюючий лептин збільшився через помірну калорійність обмеження [40]. Якби така гіпотеза була правдивою, використання метрелептину в терапії контролю ваги було б ефективним лише тоді, коли воно застосовується як доповнення до інших методів, що сенсибілізують лептин, таким чином запобігаючи метаболічній адаптації, викликаній обмеженням калорій, та сприяючи підтримці ваги.
6. Доклінічні дослідження комбінації лептину/аміліну у гризунів
Як описано вище, пов'язана з ожирінням стійкість до лептину, як видається, обумовлена дефектами дії лептину в гіпоталамусі [41,42].
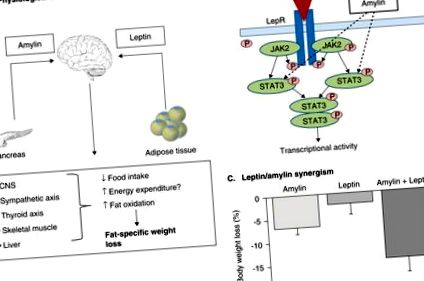
Запропонований фізіологічний ефект комбінованої терапії аміліном/лептином полягає в тому, що амілін, нейроендокринний пептид підшлункової залози, який сприяє короткочасній енергетичній регуляції, і лептин, добре встановлений гормон, який сприяє довгостроковій енергетичній регуляції, діють синергетично в ЦНС, зменшуючи споживання їжі та збільшення витрат енергії (А). У дугоподібному ядрі амілін збільшує фосфорилювання сигнального перетворювача та активатора транскрипції 3 (STAT3) сигнального шляху лептину, що призводить до збільшення або відновлення центральної чутливості до лептину [9,47] (В) і, отже, синергетичного впливу на втрату ваги, порівняно з аміліном або лептином, що вводяться окремо [10] (C).
LepR: рецептор лептину.
- Результати цілісних систем аюрведичної медицини та терапії йоги для пілотного дослідження ожиріння
- Рефлексотерапія Традиційний тайський масаж Дерев'яний релаксаційний спа-терапія Інструмент для масажу всього тіла (№5)
- Одного разу недогодовані, бідні бразильці мають нову проблему ожиріння - The Washington Post
- Стимулятор для дітей з генетичним ожирінням допомагає знизити ІМТ та апетит, результати дослідження
- Мій досвід терапії бджолиним отрутою - Ребекка Хейворд - хвороба Лайма, Великобританія