Мітохондріальна дисфункція при ожирінні: потенційна користь та механізм добавки коферменту Q10 при метаболічному синдромі
Мд Ашрафул Алам
1 Школа біомедичних наук, Університет Квінсленда, Брісбен, Австралія
2 Департамент фармацевтичних наук, Північно-Південний університет, Дакка, Бангладеш
Мд Махбубур Рахман
2 Департамент фармацевтичних наук, Північно-Південний університет, Дакка, Бангладеш
Анотація
Кофермент Q10 (Co-Q10) є важливим компонентом мітохондріального електронного транспортного ланцюга. Більшість клітин чутливі до дефіциту коферменту Q10 (Co-Q10). Цей дефіцит пов’язаний із кількома клінічними розладами, такими як серцева недостатність, гіпертонія, хвороба Паркінсона та ожиріння. Ліпідознижуючий препарат статин пригнічує перетворення HMG-CoA в мевалонат і знижує концентрацію Co-Q10 у плазмі крові. Однак добавки з Co-Q10 покращують патофізіологічний стан терапії статинами. Останні дані свідчать про те, що добавки Co-Q10 можуть бути корисними для лікування ожиріння, окисного стресу та запального процесу при метаболічному синдромі. Протизапальна реакція та ефект метаболізму ліпідів Co-Q10, ймовірно, опосередковані транскрипційною регуляцією запалення та ліпідного обміну. У цій статті розглядаються дані, що свідчать про корисну роль добавок Co-Q10 та його потенційний механізм дії на фактори, що сприяють метаболічним та серцево-судинним ускладненням.
Вступ
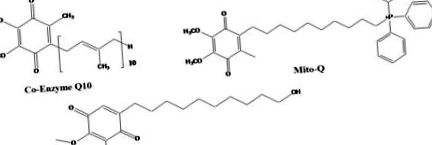
Принципова схема Co-Q10, Mito-Q та Ідебенону.
Походження, хімія та поглинання Co-Q10
Мітохондріальний біогенез та Co-Q10
Біогенез мітохондрій може модулюватися кількома регуляторами транскрипції, присутніми в клітині. Сімейство рецепторів, активованих проліфератором пероксисоми (PPAR), є таким регулятором біогенезу мітохондрій [23]. Наразі виявлено три типи білків PPAR, PPAR-α, PPAR-γ та PPAR-δ [24]. Активація PPARs також важлива для ліпідного обміну, диференціації адипоцитів та профілактики запалення [24]. Більше того, PPAR також регулюють біогенез мітохондрій через активатор, який називається активованим проліфератором пероксисоми рецептором гамма-коактиватора-1α (PGC-1α) [25,26]. PGC-1α фізіологічно регулюється фізичними вправами [27,28] та обмеженням калорій [29]. Окрім цих засобів фізичного навантаження та обмеження калорій, такі фармакологічні засоби, як фенофібрати [30] та ресвератрол [31], стимулюють PGC-1α та відновлюють мітохондріальну функцію. Активація PPARs, опосередкована Co-Q10, виявлена лише нещодавно, що було б можливим механізмом енергетичного гомеостазу в невдалих тканинах та ожирінні [32].
Порушення обміну речовин через дефіцит Co-Q10
Огашара та ін. описав перших пацієнтів (дві сестри) з первинним дефіцитом Co-Q10 у 1989 р. [33]. З раннього дитинства вони мали прогресуючу м’язову слабкість, аномальну втому та порушення функції центральної нервової системи, що характеризувалось низькою концентрацією Co-Q10 у м’язах. Обидва пацієнти помітно поліпшилися завдяки прийому всередину Co-Q10 [33]. Підтримка належного рівня Co-Q10 у всьому організмі важлива для нормальної роботи та здоров’я. Концентрація Co-Q10 у плазмі висока у здорових немовлят та дітей і з віком знижується [34,35]. Порушення обміну речовин може виникнути через дефіцит Co-Q10. Зростаючі докази свідчать, що окислювальний стрес відіграє вирішальну роль у патогенезі цукрового діабету 2 типу та його ускладнень [36]. Низькі концентрації Co-Q10 у плазмі були виявлені у пацієнтів із поганим глікемічним контролем та ускладненнями діабету [37-40].
Інгібітори HMG-CoA-редуктази (статини) знижують рівень Co-Q10 у людини [41,42]. В якості альтернативи, прийом перорального Co-Q10 може відновити рівень Co-Q10 у плазмі крові у пацієнтів, які отримують терапію статинами [41-43]. Статинічне виснаження Co-Q10 впливає на роботу м’язів. Пацієнти, які приймали статини для зменшення ліпідів у плазмі крові, страждали на міалгію та міопатичний біль [44-46]. Виснаження міокарда Co-Q10 також було продемонстровано у пацієнтів із серцевою недостатністю з кардіоміопатією, що було покращено завдяки терапії Co-Q10 [47]. Важливим фактором, що сприяє розвитку статинової міопатії, може бути генетична сприйнятливість до м’язових розладів та основні метаболічні механізми [48,49]. Завдяки терапії статинами була виявлена геномна варіація гена COQ2, який кодує пара-гідроксибензоат-поліпреніл-трансферазу для біосинтезу CoQ10 [48]. Інший звіт припускає, що статини можуть впливати на енергетичний метаболізм (дефіцит карнітинпальмітоїлтрансферази II) у поєднанні з генетичною сприйнятливістю, що викликає міопатичні наслідки у деяких пацієнтів з високим ризиком [49].
Антиоксидантна дія Co-Q10
Вплив Co-Q10 на запалення та метаболічний синдром
Окислення холестерину ліпопротеїдів низької щільності (ЛПНЩ) є ключовим регулятором розвитку запалення в клітинах ендотелію та інших тканинах [78]. Рецептор ЛПНЩ відіграє життєво важливу роль у збільшенні надходження холестерину з плазми до клітини та збільшенні кліренсу апоВ та апоЕ-містять ліпопротеїнів [79]. При цукровому діабеті та ожирінні популяції LDL-R зменшуються та підвищують рівень LDL у плазмі [80]. Миші LDLR -/- показали підвищений ліпідний профіль у плазмі та збільшення маркерів запалення у відповідь на дієту з високим вмістом жиру [79,81,82]. Антиатерогенний ефект агоніста PPARγ спостерігався у мишей LDLR -/- самців, що корелювало із покращенням чутливості до інсуліну та зниженням експресії тканин TNF-α та желатинази B [83]. Однак повідомляється, що рецептор-γ, активований проліфератором пероксисоми (PPAR-γ), послаблює запалення в активованих макрофагах, перешкоджаючи передачі сигналів NF-κB [84]. PPAR-α - ще один аналог сімейства PPAR, який також регулює протизапальні гени (рис. 2) [85].
Запропонований механізм добавки Co-Q на протизапальний та ліпідний шляхи метаболізму в тканинах у разі метаболічного синдрому. AMPK, аденозинмонофосфат-активована протеїнкіназа; PPAR, рецептор, активований проліфератором пероксисом; PGC-1α, гамма-коактиватор-1, що активується проліфератором пероксисоми; oxLDL, окислений ліпопротеїн низької щільності; NRF, коефіцієнт ядерного дихання; LXR, рецептор печінки X; Елемент відповіді PPRE PPAR.
Протизапальна активність Co-Q10 добре задокументована. Стимуляція клітин LPS призвела до чіткого вивільнення TNF-α, макрофагального запального білка-1 альфа (MIP-1α) та моноцитарного хемотрактантного білка-1 (MCP-1), які були значно ослаблені попередньою інкубацією клітин з зменшена форма Co-Q10 [86,87]. Лікування CoQ10 також зменшило підвищений рівень ліпідних профілів у плазмі та зменшило експресію мРНК прозапального цитокіну TNF-α у жировій тканині мишей ob/ob [88]. Добавки CoQ10 також покращують запальний стан у печінці щурів, що харчуються фруктами, що харчуються з високим вмістом жиру [89]. Недавні дані свідчать про те, що Co-Q10 може служити агоністом PPAR і активує опосередковану PPAR протизапальну реакцію (рис. 2) [90,91].
Вплив Co-Q10 на дисфункцію ендотелію та гіпертонію
Вплив Co-Q10 на серцеву дисфункцію
Вплив Co-Q10 на діабет та резистентність до інсуліну
Стеатоз печінки та вплив Co-Q10 на дисфункцію печінки
Добавки Co-Q10 також показали захист печінки в інших моделях порушення функції печінки. Лікування Co-Q10 показало захист печінки від токсичних ефектів печінки, спричинених ацетамінофеном, у щурів [59]. Лікування коферментом Q10 покращило обширний центрилобулярний некроз, вакуолізацію цитоплазми та балонну дегенерацію гепатоцитів із перевантаженими синусоїдами в печінці щурів [59]. Захист печінки у цих щурів залежить від блокування опосередкованих NF-kB запальних сигнальних шляхів та інактивації активності каспази [59]. Добавки Co-Q10 також ефективні для запобігання токсичному пошкодженню печінки [130]. Добавки Co-Q10 в дієті також показали захист печінки у вікових щурів завдяки посиленій клітинній антиоксидантній дії [131].
Вплив Co-Q10 на ожиріння та метаболізм жирів
Майбутні перспективи та висновок
Co-Q10 має доведений потенціал як антиоксидантної молекули з протизапальними властивостями. Недавні дані також свідчать про те, що Co-Q10 може служити активатором AMPK та PPAR і збільшує здатність клітин спалювати жир (табл. 1). Його використання все ще обмежене через погану розчинність у воді та ліпофільну природу. На сьогодні синтезовано кілька аналогів, таких як міто-Q та ідебенон.
Таблиця 1
Вплив добавок Co-Q10 на метаболізм ліпідів при метаболічному синдромі
| Ліпідний обмін | 3 преадипоцити T3-L1 | -Збільшує бета-окислення жирних кислот. | [32] |
| - ↑ Приплив Са ++; ↑ AMPK; ↑ PPAR-α. | |||
| -Запобігає диференціації адипоцитів | |||
| Щур, що годується фруктозою | -↓ Загальний холестерин; ↓ ЛПНЩ-холестерин; ↓ тригліцериди | [93] | |
| ob/ob мишей | - ↓ Загальний холестерин; ↓ тригліцериди; НЕФА | [88] | |
| - Expression експресія мРНК ліпогенних ферментів, таких як синтаза жирних кислот (FAS) та ацетил-CoA карбоксилаза 1 (ACC1). | |||
| Миші C57BL6J | - Збільшує бета-окислення жирних кислот | [90] |
Скорочення
AMPK: протеїнкіназа, що активується аденозинмонофосфатом; АТФ: аденозинтрифосфат; КАТ: Каталаза; ERK: позаклітинна рецепторна кіназа; GPx: глутатіонпероксидаза; GST: глутатіон S-трансфераза; HUVEC: ендотеліальна клітина пуповинної вени людини; IL-6: Інтерлейкін 6; IRS: субстрат рецептора інсуліну; ЛПНЩ: ліпопротеїди низької щільності; LXR: рецептор печінки X; КАРТА: Мітоген-активована протеїнкіназа; MCP-1: моноцитарний хемотаксичний білок-1; mtTFA: фактор транскрипції мітохондрій A; НІ: Оксид азоту; NRF: фактор ядерного дихання; PGC-1α: Гамма-коактиватор-1-рецептор, що активується проліфератором пероксисоми; PPAR: рецептор, активований проліфератором пероксисоми; PPRE: елемент відповіді PPAR; АФК: реактивний кисневий субстрат; СОД: Супероксиддисмутаза; STZ: Стрептозотоцин; ФНО: фактор некрозу пухлини; VSMC: судинна клітина гладких м’язів; oxLDL: окислений ліпопротеїн низької щільності; VCAM-1: молекула адгезії судинних клітин-1; UCP-1: Роз'єднання білка-1.
Конкуруючий інтерес
Автори заявляють, що у них немає жодних конкуруючих інтересів щодо цього рукопису.
Внесок авторів
MAA породила ідею, пошук літератури для огляду та склала рукопис. MMR підготував креслення, малюнки та склав рукопис. Обидва автори прочитали та схвалили остаточний рукопис.
Подяка
Ашрафула Алама підтримали стипендія доктора філософії Ісламського банку розвитку та стипендія навчання Квінслендського університету.
- Маркер запалення гіпоталамуса або механізм патогенезу ожиріння Діабет
- Чи є ожиріння причиною уникати операцій із заміщення суглобів Гарвардський журнал охорони здоров’я - Гарвардське здоров’я
- Як підземні гризуни захищають від раку Другий вид щурів-кротів має інший механізм
- Як обманні страви насправді можуть принести користь вашому харчуванню - Aaptiv
- Чи є ожиріння генетичним, що слід знати про генетику та форму ваги