Харчова поведінка при нервовій анорексії: до та після лікування
Лорел Е.С. Майєр
1 кафедра психіатрії, Коледж лікарів та хірургів, Колумбійський університет та Психіатричний інститут штату Нью-Йорк, Нью-Йорк, Нью-Йорк
Джанет Шебендах
1 кафедра психіатрії, Коледж лікарів та хірургів, Колумбійський університет та Психіатричний інститут штату Нью-Йорк, Нью-Йорк, Нью-Йорк
Ліндсей П. Боделл
2 Кафедра психології, Університет штату Флорида, Таллахассі, Флорида
Ребекка М. Шинглтон
3 кафедра психології, Бостонський університет, Бостон, штат Массачусетс
Б. Тімоті Уолш
1 кафедра психіатрії, Коледж лікарів та хірургів, Колумбійський університет та Нью-Йоркський державний психіатричний інститут, Нью-Йорк, Нью-Йорк
Анотація
Об’єктивна
Метою цього дослідження була оцінка харчової поведінки у пацієнтів з нервовою анорексією до та після нормалізації ваги та здорового контролю за допомогою стандартизованої парадигми обіднього харчування.
Метод
Вісімнадцять пацієнтів досліджували незабаром після госпіталізації та знову після набору ІМТ ≥ 19,5 кг м −2. П'ятнадцять здорових контролів вивчали двічі,
2–3 місяці.
Результати
При недостатній вазі пацієнти з АН споживали менше загальних калорій (364 ± 208 ккал) і менший відсоток калорій з жиру (18% ± 10%) порівняно з контролем (775 ± 228 ккал, р = 0,001; 38% ± 7%, р = 0,001). Після нормалізації ваги, незважаючи на помірне збільшення загальних калорій (364 ± 208 ккал проти 516 ± 273 ккал, р = 0,04) та у відсотках калорій від жиру (18% ± 10% проти 23% ± 9%, p = 0,04), пацієнти продовжували споживати менше загальних калорій і зменшений відсоток калорій з жиру порівняно з контролем (758 ± 346 ккал, p = 0,03; 38% ± 18%, p = 0,004).
Обговорення
Пацієнти з АН, навіть після гострого лікування, споживають менше загальних калорій і менше калорій з жиру, порівняно зі здоровими контролерами. Зниження загального споживання та постійне уникання жиру можуть сприяти рецидиву, а тому є потенційними терапевтичними цілями.
Вступ
Нервова анорексія (АН) - це психічне захворювання, яке характеризується низькою вагою, інтенсивним страхом набрати вагу та страхом жиру. Як основні симптоми цієї хвороби, ці страхи призводять до значних обмежень у харчуванні та втрати ваги. Лабораторні парадигми харчової поведінки постійно демонструють, що пацієнти з розладами харчової поведінки вживають патологічну харчову поведінку в лабораторних умовах1, припускаючи, що такі методи можуть бути успішно використані для дослідження клінічних припущень. Однак більшість опублікованих досліджень обстежували пацієнтів з АН, хворих на гостру хворобу та недостатню вагу. 2–4
Використовуючи одноразовий прийом їжі, Sysko et al. 5 описано, що пацієнти з АН споживали менше калорій при недостатній вазі порівняно з контролем. Незважаючи на збільшення ваги, що перевищує 90% ідеальної маси тіла (IBW), споживання не суттєво збільшилось і залишилось зниженим порівняно зі здоровим контролем. Визнаним обмеженням дослідження було використання одноразового полунично-йогуртового коктейлю як проксі для «їжі».
У поточному дослідженні використовувалася парадигма прийому їжі з декількох елементів для оцінки харчової поведінки до та після нормалізації ваги у пацієнтів, госпіталізованих для лікування АН та у здорових людей контролю.
Метод
Це дослідження було схвалено Державним психіатричним інститутом штату Нью-Йорк (NYSPI)/Колумбійським університетом Департаменту з питань психіатрії. Усі учасники надали інформовану згоду перед вступом у дослідження.
Учасниками були 25 пацієнтів (23 жінки, 2 чоловіки), які відповідали критеріям DSM-IV 6 щодо АН, за винятком аменореї та 20 здорових контролерів подібного віку, статі та ІМТ пацієнтів з відновленою вагою. Усі учасники не мали ліків, крім ацетамінофену та ібупрофену, щонайменше за 2 тижні до початкового тестування.
Пацієнти з АН були прийняті на лікування до стаціонарної служби розладу харчування в Медичному центрі NYSPI/Колумбійського університету. Лікування включало структуровану поведінкову програму, спрямовану на нормалізацію ваги та режиму харчування. 7 Пацієнтів регулярно зважували і, як очікувалося, вони набирали щонайменше 1 кг на тиждень. Калорійність починалася з 1800 ккал на день і була збільшена на
400 ккал на день –1 через день, доки не буде призначено 3000 ккал у їжі та 720 ккал у харчовій добавці (Ensure або Ensure Plus; Ross Nutritional, Columbus, OH). За потреби додавались додаткові калорії у вигляді рідкої харчової добавки. Фаза збільшення ваги тривала, поки пацієнти не досягли 90% ІБВ. 8
Особи з АН вивчалися протягом перших двох тижнів госпіталізації, до початку формального набору ваги, і знову після досягнення щонайменше 90% IBW. Здоровий контроль також вивчали двічі,
З інтервалом у 2-3 місяці, подібно до інтервалу між дослідженнями пацієнтів.
На ранок тестування (
8 ранку), учасники їли стандартний сніданок
300 ккал, а потім не мали нічого їсти та пити до пробного обіду (
13:00). Лабораторна обідня їжа складалася з 25 продуктів, поставлених на стіл: курка на грилі, смажена курка, макарони та сир, риба тунця, соління, картопля фрі, салат, шоколадне печиво-сендвіч, шоколадна плитка, морозиво, пончики, попкорн, фруктовий салат, скибочки цільної пшениці та білого хліба, вершкове масло, гірчиця, майонез, кетчуп, заправка з італійських салатів, сіль, перець, холодний чай, вода у пляшках та дієтична кола. Учасники отримали вказівку: ‘‘ Це ваш обід на день. Їжте скільки завгодно або мало, як хотіли ''. Під час їжі вони були самі в кімнаті, за ними спостерігали за одностороннім, замкнутим телевізором. Учасники мали їсти їжу до 60 хв. Їх просили вказати, коли вони закінчили їжу, подзвонивши на стіл. Відразу після їжі, поки вони все ще сиділи за столом, учасників попросили оцінити загальну кількість споживаних калорій.
Вага грамів та ккал були розраховані для всієї споживаної їжі, а також складу макроелементів їжі, включаючи грами вуглеводів (CHO), білка (PRO) та жиру (FAT). Розраховано показник щільності енергетичної дієти, який визначається як споживання (ккал), поділене на вагу (г) споживаної їжі та напоїв. 9 Дієтичний показник різноманітності, визначений як сукупна кількість різних калорійних продуктів харчування та напоїв. 9
ТАБЛИЦЯ 1
Дані демографічної та прийомової поведінки з лабораторної оцінки багаторазового прийому їжі до та після нормалізації ваги у пацієнтів з АН порівняно зі здоровими контролями, що вивчались двічі
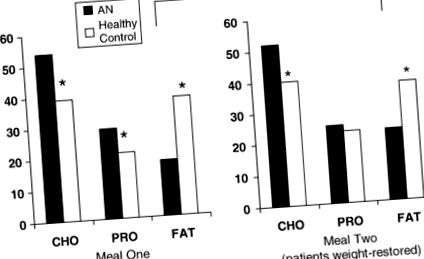
Повторний аналіз заходів виявив значущі відмінності між групами споживання (F = 15,93, p Таблиця 1 ). Відсоток калорій від CHO та PRO був значно вищим, а відсоток споживаних калорій як FAT був значно нижчим у пацієнтів порівняно з контролем ( Рис. 1 ).
Середній відсоток калорій з вуглеводів (CHO), білків (PRO) та жирів (FAT), що вживаються пацієнтами з АН та здоровим контролем під час кожного лабораторного прийому їжі.
* У порівнянні зі здоровими людьми, пацієнти з АН споживали більший відсоток калорій від CHO (p Таблиця 1 ). Середнє надмірне або занижене споживання калорій не змінювалось від прийому їжі до їжі дві в будь-якій групі.
Не було суттєвих відмінностей щодо будь-яких показників харчової поведінки між підтипами обмеження та переїдання/очищення (дані не наведені).
Обговорення
У поточному дослідженні пацієнти з АН, навіть після гострого лікування та відновлення нормальної маси тіла, споживають менше загальних калорій і менше калорій з жиру, порівняно зі здоровим контролем. Хоча споживання збільшується із відновленням ваги, воно залишається значно зменшеним порівняно з контролем.
Це дослідження узгоджується з результатами Sysko et al. 5 зменшення споживання полуничного йогуртового коктейлю у пацієнтів з АН порівняно з контролем до та після гострого лікування, і поширює їх результати на шведський стіл із кількох страв. На відміну від дослідження Сіско, пацієнти з АН у цьому дослідженні змогли помірковано збільшити споживання із збільшенням ваги. Однак в обох дослідженнях споживання не вдалося повністю нормалізувати.
Інші особливості дієти - споживання макроелементів, щільність енергії та різноманітність дієти - також відрізнялися між пацієнтами та контролем. Більш низькі показники енергетичної щільності можуть відображати як поведінкове уникання дієтичного жиру, оскільки пацієнти з низькою вагою і після відновлення ваги споживали менше грамів жиру, так і збільшення споживання неживних напоїв (наприклад, води, дієтичної газованої води). Наші висновки щодо уникнення жиру та зниженої енергетичної щільності при недостатній вазі узгоджуються з клінічними спостереженнями та попередніми дослідженнями спостережуваного споживання, 2–4, і поширюють результати на нещодавно відновлених вагою осіб. Постійність такого режиму харчування може сприяти ускладненню збереження ваги. 9
В рамках протоколу стаціонарного лікування пацієнтам призначають
4000 ккал на день у вигляді триразового харчування (
900 ккал кожен) плюс одна закуска (
300 ккал) щодня, плюс мінімум 720 ккал рідкої добавки, і пацієнти повинні їсти 100% їжі. Розподіл макроелементів у госпітальній дієті становить 55–60% вуглеводів, 15–20% білків та
30% жиру. До моменту другої лабораторної оцінки їжі пацієнти регулярно та успішно виконували ці страви протягом багатьох тижнів у контексті структурованого поведінкового протоколу. Слід зазначити - і потенційне занепокоєння - що за тимчасової відсутності такої структури споживання калорій зменшується, а поведінкове уникнення харчових жирів є очевидним.
Рецидив є значною проблемою при лікуванні АН. Понад 50% пацієнтів рецидивують протягом року після госпіталізації в стаціонар. 10 Передбачити, хто рецидивує, є складним завданням. У великому багатопрофільному дослідженні щодо профілактики рецидивів було розглянуто 11 численних психологічних факторів, включаючи депресію, тривогу, прийом їжі, проблеми, пов’язані з формою та вагою та прихильність до фізичних вправ, як потенційні провісники відмови утримувати нормальну вагу протягом 6 місяців після лікарні розряд. 12 Тільки ІМТ при рандомізації та швидкість втрати ваги протягом перших 4 тижнів після виписки були значущими предикторами. У відповідному дослідженні Schebendach et al. 9 виявили, що знижена щільність енергетичної дієти та різноманітність дієт у нещодавно відновлених вагою пацієнтів до виписки з лікарні були пов’язані з поганим результатом у наступному році після виписки. Підсумовуючи, оскільки втрата ваги повинна бути пов’язана з недостатнім споживанням їжі щодо витрат енергії, ці дані настійно свідчать про те, що стійкі порушення в харчовій поведінці є ключовим елементом вразливості до рецидивів і можуть бути конкретною метою для втручання.
Пацієнти з АН часто здаються дуже обізнаними щодо поживності та калорійності продуктів. Наше дослідження підтверджує, що пацієнти з АН завищують споживання калорій. 2 Неодноразово завищене споживання може схилити пацієнтів до рецидиву, оскільки це може сприяти помилковому висновку пацієнтів про те, що вони дотримувались своїх калорій.
Сильні сторони поточного дослідження включають парадигму прийому їжі з кількома елементами (на відміну від окремих позицій). Ця конструкція дозволила представити висококалорійні та низькокалорійні (наприклад, смажену курку та курку на грилі) або більше, ніж менш «здорові» (наприклад, цільна пшениця проти білого хліба) варіанти їжі, щоб викликати перевагу пацієнта. Всіх учасників двічі вивчали, щоб контролювати ефект часу та новизну подання фуршету. Відсутність суттєвих змін у споживанні та змісті їжі контролерів свідчить про значну надійність тестування та повторного тестування.
Однак, невід'ємною частиною дизайну дослідження їжі є також обмеження, які слід визнати. Лабораторне харчування не є обстановкою `` реального світу '', а презентація "шведський стіл" не є типовою для середнього прийому їжі. Учаснику було доступно більше їжі, ніж очікувалося спожити, що, можливо, збільшило тривожність як пацієнта, так і контролю. Знання, що за ними спостерігають по замкнутому телебаченню, могло мати вплив на споживання. Навіть за інструкцією «обідня їжа» двоє пацієнтів переїдали під час сеансу. Незважаючи на ці обмеження, ця парадигма видається потенційно цінним методом оцінки поведінкових порушень, критичних для розвитку та підтримки АН.
Висновок
Пацієнти з АН споживають менше калорій і уникають харчових жирів у порівнянні зі здоровими контролерами як до, так і після відновлення ваги. Зниження загального споживання та стійке поведінкове уникнення жиру може сприяти ризику рецидивів, а тому є потенційною метою для втручання в лікування.
Подяки
Автори дякують Евелін Аттіа, Майклу Девліну та Джоанні Штейнгласс за їх вдумливі редакторські коментарі. Вони також дякують пацієнтам та працівникам GCRU, включаючи Мері Бонгьові, Дена Ріхтера та Арлін Болсон, без участі та підтримки цього дослідження не могло б відбутися.
За підтримки Інституту клінічних та трансляційних досліджень Ірвінга; Пілотна премія за клінічні випробування; Програма вчених Ірвінга в Колумбійському університеті; AstraZeneca.
Виноски
Обов'язки авторів полягали в наступному: Концепція та дизайн дослідження: LESM, JS, BTW; Збір даних: LESM, JS, LPB; Аналіз та інтерпретація даних: LESM, JS, LPB, RMS, BTW; Підготовка рукописів: LESM, JS, LPB, RMS, BTW. Усі автори несуть відповідальність за цілісність даних та точність їх аналізу.
- Харчова поведінка впливає на якість життя при цукровому діабеті 2 типу SpringerLink
- Харчова поведінка у зразку надмірної ваги та ожиріння Дослідження поперечного перерізу
- Терапія лікування розладів харчування Приоритетна група
- Люди, які страждають на порушення харчування, використовуючи енергетичні напої як заміну їжі, - Центр лікування Fairwinds
- Харчова поведінка після баріатричної хірургії (EBBS) Опитувальник - новий перевірений інструмент для кількісної оцінки